题目内容
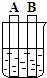
 (2008?海淀区一模)张老师利用右图装置为同学们做了一个兴趣实验.a是气球,b中放入白色的碳酸钡固体,c、d是胶头滴管,d中吸入氢氧化钠的浓溶液.
(2008?海淀区一模)张老师利用右图装置为同学们做了一个兴趣实验.a是气球,b中放入白色的碳酸钡固体,c、d是胶头滴管,d中吸入氢氧化钠的浓溶液.(1)首先将滴管c中的液体挤入集气瓶b中,观察到气球涨大,b中白色固体消失,则c中液体的名称可能为
盐酸
盐酸
(只写一种),其反应的化学方程式为BaCO3+2HCl=BaCl2+H2O+CO2↑
BaCO3+2HCl=BaCl2+H2O+CO2↑
;(2)然后将滴管d中的液体挤入集气瓶b中,可以观察到的现象是
气球缩小,有白色沉淀生成
气球缩小,有白色沉淀生成
,与此现象有关反应的化学方程式为CO2+2NaOH=Na2CO3+H2O,Na2CO3+BaCl2=BaCO3↓+2NaCl
CO2+2NaOH=Na2CO3+H2O,Na2CO3+BaCl2=BaCO3↓+2NaCl
.分析:(1)根据碳酸盐与酸反应生成二氧化碳气体分析;
(2)根据氢氧化钠和二氧化碳反应生成碳酸钠和水以及碳酸钠和氯化钡反应生成白色的碳酸钡沉淀和氯化钠进行分析;
(2)根据氢氧化钠和二氧化碳反应生成碳酸钠和水以及碳酸钠和氯化钡反应生成白色的碳酸钡沉淀和氯化钠进行分析;
解答:解:(1)因为碳酸钡和稀盐酸反应生成氯化钡、水和二氧化碳,故填:盐酸;BaCO3+2HCl=BaCl2+H2O+CO2↑
(2)氢氧化钠和二氧化碳反应生成碳酸钠和水,碳酸钠和氯化钡反应生成白色的碳酸钡沉淀和氯化钠,二氧化碳被消耗,瓶内气体压强变小,所以气球缩小,故填:气球缩小,有白色沉淀生成;CO2+2NaOH=Na2CO3+H2O,Na2CO3+BaCl2=BaCO3↓+2NaCl
(2)氢氧化钠和二氧化碳反应生成碳酸钠和水,碳酸钠和氯化钡反应生成白色的碳酸钡沉淀和氯化钠,二氧化碳被消耗,瓶内气体压强变小,所以气球缩小,故填:气球缩小,有白色沉淀生成;CO2+2NaOH=Na2CO3+H2O,Na2CO3+BaCl2=BaCO3↓+2NaCl
点评:本题考查了酸的化学性质,酸和碳酸盐反应生成二氧化碳气体是检验碳酸根离子的方法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 (2008?海淀区一模)A、B、C、D、E是初中化学中常见的物质,其转化关系如图所示(产物中的某些物质可能略去).请依据转化关系图,写出符合要求的一组答案.
(2008?海淀区一模)A、B、C、D、E是初中化学中常见的物质,其转化关系如图所示(产物中的某些物质可能略去).请依据转化关系图,写出符合要求的一组答案. (2008?海淀区一模)某实验小组模拟高炉炼铁的化学反应原理进行实验,其装置如下图所示,请回答下列问题.
(2008?海淀区一模)某实验小组模拟高炉炼铁的化学反应原理进行实验,其装置如下图所示,请回答下列问题. (2008?海淀区一模)小东和小明收集了两个形状、大小、轻重和硬度均不同的易拉罐,如图所示.他们很想知道每个易拉罐的材料成分,于是展开了以下探究过程.
(2008?海淀区一模)小东和小明收集了两个形状、大小、轻重和硬度均不同的易拉罐,如图所示.他们很想知道每个易拉罐的材料成分,于是展开了以下探究过程.