题目内容
16.高锰酸钾是锰的重要化合物和常用的氧化剂.如图所示是工业上用软锰矿制备高锰酸钾的一种工艺流程.
(1)写出实验室用KMnO4制备气体的一个化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(2)操作Ⅰ的名称是过滤.
(3)上述流程中可以循环使用的物质有MnO2KOH(至少填两种).
(4)用结晶法分离KMnO4、K2CO3两种物质,进行该操作前需查阅的资料是两种物质的溶解度,KMnO4粗品制成精品,须进行洗涤再干燥,检查是否洗净的具体操作是取最后一次的洗涤液少量,加入CaCl2溶液,若没有白色沉淀生成,说明洗涤干净.
分析 ( )实验室用KMnO4制取O2,高锰酸钾受热分解生成锰酸钾、二氧化锰、氧气,据此解答;
(2)分离固体与溶液,采用过滤操作;
(3)最初反应物中和最终生成物中含有的物质就能循环利用;
(4)用结晶法分离固体混合物,要知道固体的溶解度,检验高锰酸钾的洗涤液中是否含有碳酸钾.
解答 解:(1)高锰酸钾受热分解生成锰酸钾、二氧化锰、氧气,故填:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(2)该操作是分离固体与溶液,是过滤操作,故填:过滤;
(3)在开始的反应物和最终的生成物中都含有MnO2和KOH,所以二氧化锰和氢氧化钾能循环使用,故答案为:MnO2 KOH;
(4)要知道KMnO4、K2CO3两种物质的溶解度才能选择结晶法分离,检查高锰酸钾是否洗净就是检验是否还有碳酸钾,可加入氯化钙溶液,观察是否生产白色沉淀.
故填:两种物质的溶解度;取最后一次的洗涤液少量,加入CaCl2溶液,若没有白色沉淀生成,说明洗涤干净.
点评 本题考查对工艺流程的理解、阅读题目获取信息的能力等,解答本题时要充分理解图中提供的信息,只有理解了图中信息才能对问题做出正确的判断,题目难度中等.

练习册系列答案
相关题目
2. 在激烈的足球比赛中,运动员受到轻伤时,用氯乙烷喷雾剂向伤口喷射,可减轻运动员疼痛,如图是氯乙烷的分子模型,下列说法中错误的是( )
在激烈的足球比赛中,运动员受到轻伤时,用氯乙烷喷雾剂向伤口喷射,可减轻运动员疼痛,如图是氯乙烷的分子模型,下列说法中错误的是( )
 在激烈的足球比赛中,运动员受到轻伤时,用氯乙烷喷雾剂向伤口喷射,可减轻运动员疼痛,如图是氯乙烷的分子模型,下列说法中错误的是( )
在激烈的足球比赛中,运动员受到轻伤时,用氯乙烷喷雾剂向伤口喷射,可减轻运动员疼痛,如图是氯乙烷的分子模型,下列说法中错误的是( )| A. | 氯乙烷属于有机物 | |
| B. | 氯乙烷是由三种元素组成的 | |
| C. | 氯乙烷的化学式为C2H5Cl | |
| D. | 氯乙烷气体是由碳原子、氢原子、氯原子构成的 |
7.下列有关纯碱的说法正确的是( )
| A. | 用pH试纸测出纯碱溶液的pH值为7 | |
| B. | 纯碱溶液可以含有Ca2+的溶液发生复分解反应 | |
| C. | 侯氏制碱法中的纯碱指氢氧化钠 | |
| D. | 纯碱中含有少量的小苏打可以用稀盐酸除去 |
4.下列发生化学变化的是( )
| A. |  食品充氮防腐 | B. |  含氢氧化钠的炉具清洁剂去油污 | ||
| C. | 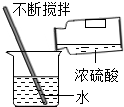 稀释浓硫酸 | D. | 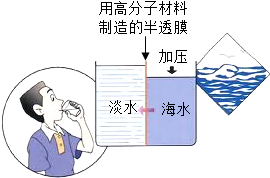 高分子分离膜淡化海水 |
1. 我校化学兴趣小组在探究金属与盐溶液反应时,发现金属钠放在硫酸铜溶液中有气泡和沉淀产生,为了探究生成的气体和固体沉淀的成分与沉淀的原因,进行如下实验:
我校化学兴趣小组在探究金属与盐溶液反应时,发现金属钠放在硫酸铜溶液中有气泡和沉淀产生,为了探究生成的气体和固体沉淀的成分与沉淀的原因,进行如下实验:
【提出问题】产生的气体是什么?
【猜想与假设】(1)二氧化硫;(2)二氧化碳;(3)氢气.你认为不合理的猜想是(2)二氧化碳,
【查阅资料】①二氧化硫与二氧化碳化学性质相似,都能与澄清石灰水反应生成白色沉淀.②钠是一种非常活泼的金属,能与冷水剧烈反应,化学方程式为2Na+2H2O═2NaOH+H2↑.
【方案设计】依据上述猜想设计了如下实验方案:
(1)甲同学验证生成的气体是否为二氧化硫,将生成的气体通入澄清的石灰水中,发现澄清石灰水未浑浊,确定生成的气体不是二氧化硫.
(2)乙同学利用如图所示装置验证生成的气体是氢气.实验过程中可发现到玻璃管中的现象是黑色氧化铜变成红色,化学方程式为H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O.
【得出结论】猜想(3)正确.
【拓展延伸】钠和硫酸铜溶液反应生成的沉淀是什么?
【分析讨论】认为钠可能会与水反应生成氢氧化钠和氢气,氢氧化钠再与硫酸铜反应生成蓝色的氢氧化铜沉淀.
(3)丙同学认为:除了上述反应,可能钠直接与硫酸铜反应生成红色的单质铜,只是蓝色的氢氧化铜沉淀掩盖了红色的铜.请你设计实验证明该蓝色沉淀中不含单质铜.
(4)有上述探究,同学们认为硫酸铜溶液可能显酸性(填“酸性”、“中性”或“碱性”),可以选择紫色石蕊试液(填试剂的名称)来验证.
 我校化学兴趣小组在探究金属与盐溶液反应时,发现金属钠放在硫酸铜溶液中有气泡和沉淀产生,为了探究生成的气体和固体沉淀的成分与沉淀的原因,进行如下实验:
我校化学兴趣小组在探究金属与盐溶液反应时,发现金属钠放在硫酸铜溶液中有气泡和沉淀产生,为了探究生成的气体和固体沉淀的成分与沉淀的原因,进行如下实验:【提出问题】产生的气体是什么?
【猜想与假设】(1)二氧化硫;(2)二氧化碳;(3)氢气.你认为不合理的猜想是(2)二氧化碳,
【查阅资料】①二氧化硫与二氧化碳化学性质相似,都能与澄清石灰水反应生成白色沉淀.②钠是一种非常活泼的金属,能与冷水剧烈反应,化学方程式为2Na+2H2O═2NaOH+H2↑.
【方案设计】依据上述猜想设计了如下实验方案:
(1)甲同学验证生成的气体是否为二氧化硫,将生成的气体通入澄清的石灰水中,发现澄清石灰水未浑浊,确定生成的气体不是二氧化硫.
(2)乙同学利用如图所示装置验证生成的气体是氢气.实验过程中可发现到玻璃管中的现象是黑色氧化铜变成红色,化学方程式为H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O.
【得出结论】猜想(3)正确.
【拓展延伸】钠和硫酸铜溶液反应生成的沉淀是什么?
【分析讨论】认为钠可能会与水反应生成氢氧化钠和氢气,氢氧化钠再与硫酸铜反应生成蓝色的氢氧化铜沉淀.
(3)丙同学认为:除了上述反应,可能钠直接与硫酸铜反应生成红色的单质铜,只是蓝色的氢氧化铜沉淀掩盖了红色的铜.请你设计实验证明该蓝色沉淀中不含单质铜.
| 实验步骤 | 实验现象 | 实验结论 |
该蓝色沉淀中不含不含单质铜 |


