题目内容
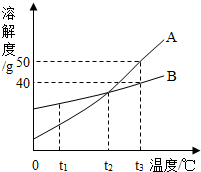 图是A、B两种物质的溶解度曲线,请回答:
图是A、B两种物质的溶解度曲线,请回答:(1)t1℃时,A、B两种物质溶解度的大小关系为A
(2)t3℃时,把26g固体A放入50g水中,充分溶解后可得到A的
(3)固体A中混有少量B,可采用
(4)在其他条件不变的情况下,若把tl℃时A、B的饱和溶液分别升温至
t2℃,此时两种溶液中溶质的质量分数的大小关系为A
t3℃时A、B的饱和溶液分别降温至t2℃,此时两种溶液中溶质的质量分数的大小关系为A
考点:固体溶解度曲线及其作用,结晶的原理、方法及其应用,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:(1)据溶解度曲线可比较同一温度时物质的溶解度大小;
(2)t3℃时,A物质的溶解度为50g,即100g水中最多溶解50g溶质,所以50g水中只能溶解25g溶质,把26g固体A放入50g水中,充分溶解后可得到A的饱和溶液;
(3)据AB的溶解度受温度影响程度分析提纯A的方法.
(4)t1℃时,B的溶解度大于A的溶解度,且A、B两物质的溶解度随温度升高而增大,把tl℃时A、B的饱和溶液分别升温至t2℃,此时两种溶液中溶质的质量分数的大小关系为A<B;
饱和溶液中溶解度相等则溶质的质量分数也相等;
(2)t3℃时,A物质的溶解度为50g,即100g水中最多溶解50g溶质,所以50g水中只能溶解25g溶质,把26g固体A放入50g水中,充分溶解后可得到A的饱和溶液;
(3)据AB的溶解度受温度影响程度分析提纯A的方法.
(4)t1℃时,B的溶解度大于A的溶解度,且A、B两物质的溶解度随温度升高而增大,把tl℃时A、B的饱和溶液分别升温至t2℃,此时两种溶液中溶质的质量分数的大小关系为A<B;
饱和溶液中溶解度相等则溶质的质量分数也相等;
解答:解:(1)t1℃时,A的溶解度小于B物质的溶解度;
(2)t3℃时,A物质的溶解度为50g,即100g水中最多溶解50g溶质,所以50g水中只能溶解25g溶质,把26g固体A放入50g水中,充分溶解后可得到A的饱和溶液;
(3)A的溶解度受温度影响较大,B的溶解度受温度影响较小,所以若A中混有少量B,欲得到较纯净的A,可以采用降温结晶的方法;
(4)t1℃时,B的溶解度大于A的溶解度,且A、B两物质的溶解度随温度升高而增大,把tl℃时A、B的饱和溶液分别升温至t2℃,此时两种溶液中溶质的质量分数的大小关系为A<B;
t2℃时,A、B两种物质的溶解度相等,所以饱和溶液中溶质质量分数也相等;
故答案为:(1)<;(2)=;(3)冷却热饱和溶液(或降温结晶).
答案为:(1)<(2)饱和 (3)降温结晶法 (4)B>A=
(2)t3℃时,A物质的溶解度为50g,即100g水中最多溶解50g溶质,所以50g水中只能溶解25g溶质,把26g固体A放入50g水中,充分溶解后可得到A的饱和溶液;
(3)A的溶解度受温度影响较大,B的溶解度受温度影响较小,所以若A中混有少量B,欲得到较纯净的A,可以采用降温结晶的方法;
(4)t1℃时,B的溶解度大于A的溶解度,且A、B两物质的溶解度随温度升高而增大,把tl℃时A、B的饱和溶液分别升温至t2℃,此时两种溶液中溶质的质量分数的大小关系为A<B;
t2℃时,A、B两种物质的溶解度相等,所以饱和溶液中溶质质量分数也相等;
故答案为:(1)<;(2)=;(3)冷却热饱和溶液(或降温结晶).
答案为:(1)<(2)饱和 (3)降温结晶法 (4)B>A=
点评:本题主要考查了学生对溶解度曲线知识的掌握和简单应用,难度不大.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目
分析下列四个选项中化学不涉及的研究领域是( )
| A、开发洁净能源 |
| B、物质气、液、固三态互变的条件 |
| C、合成新的物质 |
| D、防治环境污染 |
将锌片分别放入下列各溶液中,反应后所得溶液的质量减小的是( )
| A、硫酸铜溶液 | B、稀硫酸 |
| C、硫酸镁溶液 | D、硝酸银溶液 |
元素的性质特别是其化学性质有密切联系的是( )
| A、质子数 | B、中子数 |
| C、核外电子数 | D、最外层电子数 |
下列变化中属于化学变化的是( )
| A、榨取果汁 |
| B、粉碎废纸 |
| C、太阳能热水器中冷水变热水 |
| D、在催化剂作用下太阳能光解水制氢 |