��Ŀ����
�⻯�ƣ�CaH2��������һ�ִ�����ϣ��ǵ�ɽ�˶�Ա���õ���Դ�ṩ�������Ķ����ϡ��ټ�ʯ���������ƺ��������ƵĻ����ڸ���ˮ�����������ҷ�Ӧ�����������ƺ����������⻯��Ҫ�ܷⱣ�棬��ˮ��Ӧ�����������ƺ�������
���⻯�Ƶ��Ʊ����⻯��ͨ����������Ƽ����Ƶã�ij�о�����Ƶ���ȡװ����ͼ1��ʾ���̶�װ��ʡ�ԣ�
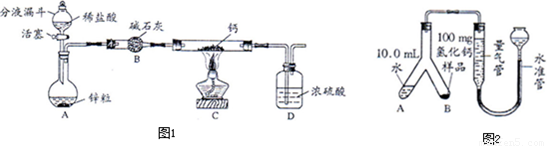
�ش��������⣺
��1��ͼ1װ��A����ȡ�����Ļ�ѧ����ʽΪ______��
��2��װ��B��������______��
��3��װ��C����ȡ�⻯�ƵĻ�ѧ����ʽΪ______ CaH2
���𰸡���������1������п����ϡ���ᷴӦԭ����д����ʽ����2�����ݼ�ʯ�ҵijɷֺ��������ʵ����ʷ�����𣻣�3�����ݷ�Ӧ�������ͷ�Ӧ������д����ʽ����4������װ���ص���⻯����ˮ��Ӧ�����������з�������5��������������ڷ�Ӧǰ��Һ����6����������������=���������×�������ܶ�����������������ٽ���⻯����ˮ��Ӧ����ʽ������ˮ��Ӧ����ʽ������⻯�Ƶ�����������������Ʒ���⻯�ƵĴ��ȣ�
����⣺��1��п����ϡ���ᷴӦ�����Ȼ�п���������ù۲취��ƽ����Ӧ�ķ���ʽ�ǣ�Zn+2HCl=ZnCl2+H2����
��2����ʯ���������ƺ��������ƵĻ�����������ˮ�ɷ�Ӧ���������ƿ�������������������ܷ�Ӧ�����Ը�װ�õ�����������ˮ�����Ͳ����Ȼ������壻
��3���ƺ������ڼ��ȵ������������⻯�ƣ�����ʽ��Ca+H2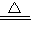 CaH2��
CaH2��
��4�������⻯����ˮ��Ӧ���������������ж���Ʒ��ˮ�Ƿ���ȫ��Ӧ�����Թ۲��ұߵ���������Һ�棬�����ٱ仯��������ȫ��Ӧ��
��5��������������ڷ�Ӧǰ��Һ��Ϊ��110.0mL-10.0mL=100.0mL��
��6����Ӧ���������������ǣ�100.0mL×0.09mg/mL=9mg
����Ʒ���⻯�Ƶ�������X��������������ΪY����Ƶ�����Ϊ100mg-X������ˮ��Ӧ������������Ϊ9mg-Y��
CaH2+2H2O�TCa��OH��2+2H2��
42 4
X Y
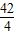 =
=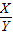 ���Y=
���Y=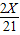
Ca+2H2O�TCa��OH��2+H2��
40 2
100mg-X 9mg-Y
���ݣ�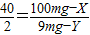 ��Y=
��Y=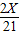 ���룬���X=88.4mg
���룬���X=88.4mg
������Ʒ���⻯�ƵĴ���Ϊ��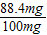 ×100%=88.4%��
×100%=88.4%��
�ʴ�Ϊ����1��Zn+2HCl=ZnCl2+H2������2������ˮ�����Ͳ����Ȼ������壻��3��Ca+H2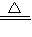 CaH2����4���۲��ұߵ���������Һ�棬�����ٱ仯��������ȫ��Ӧ����5��100.0����6��88.4%��
CaH2����4���۲��ұߵ���������Һ�棬�����ٱ仯��������ȫ��Ӧ����5��100.0����6��88.4%��
���������⿼������ȫ����ۺϣ����ʱҪ�������֪ʶϸ�ķ�����������Ǽ����⣬�ܺܺõĿ���ѧ����֪ʶ�����պ�Ӧ��������
����⣺��1��п����ϡ���ᷴӦ�����Ȼ�п���������ù۲취��ƽ����Ӧ�ķ���ʽ�ǣ�Zn+2HCl=ZnCl2+H2����
��2����ʯ���������ƺ��������ƵĻ�����������ˮ�ɷ�Ӧ���������ƿ�������������������ܷ�Ӧ�����Ը�װ�õ�����������ˮ�����Ͳ����Ȼ������壻
��3���ƺ������ڼ��ȵ������������⻯�ƣ�����ʽ��Ca+H2
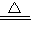 CaH2��
CaH2����4�������⻯����ˮ��Ӧ���������������ж���Ʒ��ˮ�Ƿ���ȫ��Ӧ�����Թ۲��ұߵ���������Һ�棬�����ٱ仯��������ȫ��Ӧ��
��5��������������ڷ�Ӧǰ��Һ��Ϊ��110.0mL-10.0mL=100.0mL��
��6����Ӧ���������������ǣ�100.0mL×0.09mg/mL=9mg
����Ʒ���⻯�Ƶ�������X��������������ΪY����Ƶ�����Ϊ100mg-X������ˮ��Ӧ������������Ϊ9mg-Y��
CaH2+2H2O�TCa��OH��2+2H2��
42 4
X Y
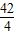 =
=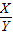 ���Y=
���Y=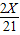
Ca+2H2O�TCa��OH��2+H2��
40 2
100mg-X 9mg-Y
���ݣ�
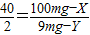 ��Y=
��Y=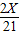 ���룬���X=88.4mg
���룬���X=88.4mg������Ʒ���⻯�ƵĴ���Ϊ��
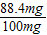 ×100%=88.4%��
×100%=88.4%���ʴ�Ϊ����1��Zn+2HCl=ZnCl2+H2������2������ˮ�����Ͳ����Ȼ������壻��3��Ca+H2
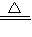 CaH2����4���۲��ұߵ���������Һ�棬�����ٱ仯��������ȫ��Ӧ����5��100.0����6��88.4%��
CaH2����4���۲��ұߵ���������Һ�棬�����ٱ仯��������ȫ��Ӧ����5��100.0����6��88.4%�����������⿼������ȫ����ۺϣ����ʱҪ�������֪ʶϸ�ķ�����������Ǽ����⣬�ܺܺõĿ���ѧ����֪ʶ�����պ�Ӧ��������

��ϰ��ϵ�д�
�����Ŀ

