题目内容
12. 实验室保存-瓶浓盐酸,瓶上的标签部分内容如图所示,请根据标签上的信息回答下列各问:
实验室保存-瓶浓盐酸,瓶上的标签部分内容如图所示,请根据标签上的信息回答下列各问:(1)这-瓶浓盐酸中溶质的质量是多少克?(结果精确到0.1)
(2)取100克此瓶内的浓盐酸可以稀释成1.85%的稀盐酸多少克?同时加水多少克?
分析 (1)根据溶质质量=溶液质量×溶质的质量分数,进行分析解答.
(2)根据溶液稀释前后溶质的质量不变,结合题意进行分析解答.
解答 解:(1)500mL=500cm3,这-瓶浓盐酸中溶质的质量是1.19g/cm3×500cm3×37%≈220.2g.
(2)设可以稀释成1.85%的稀盐酸的质量为x,根据溶液稀释前后溶质的质量不变,
则100g×37%=x×1.85% x=2000g.
同时加水的质量为2000g-100g=1900g.
答:(1)这-瓶浓盐酸中溶质的质量是220.2g;(2)可以稀释成1.85%的稀盐酸2000g,同时加水1900g.
点评 本题难度不大,掌握溶质质量=溶液质量×溶质的质量分数、溶液稀释前后溶质的质量不变是正确解答本题的关键.

练习册系列答案
 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
20.今年是扬州市2500年城庆.“人文古扬州,诗画瘦西湖”,本着“治城先治水”的理念,通过清水活水工程,瘦西湖水质有了显著改善.某中学化学兴趣小组对瘦西湖水进行了如下探究:取样→操作Ⅰ→后续检测
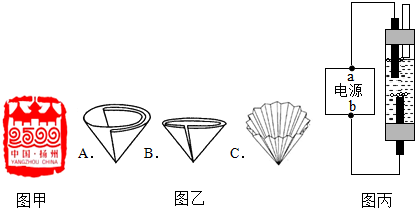
(1)操作Ⅰ是过滤,所需的玻璃仪器有烧杯、玻璃棒、漏斗,玻璃棒在过滤中的作用是引流.过滤操作中滤纸有多种折法,为了加快过滤速率,如图乙,你选择折法是A.
下表是检测报告的一部分.
(2)感官指标表现的是自来水的物理(填“物理”或“化学”)性质.
(3)化学指标中的铜、铁是指元素(填“元素”或“单质”),水中的“铁”以铁离子形式存在,铁离子的符号是Fe3+.
(4)“pH”指标表示酸碱性:若pH=7,表示中性;pH<7,表示酸性;pH>7,表示碱性.检测报告表明瘦西湖水呈碱性(填“酸性”“碱性”或“中性”).
(5)实验室用瘦西湖水制取蒸馏水的方法是D.
A.吸附 B.沉淀 C.过滤 D.蒸馏
(6)如图丙是一种家用环保型消毒液发生器,其中发生的主要反应是氯化钠和水在通电条件下反应生成氢氧化钠(NaOH)和两种气体单质(其中一种是最轻的气体),该反应的化学式表达式为2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑;从能量变化角度看,该反应将电能转化为化学能.
(1)操作Ⅰ是过滤,所需的玻璃仪器有烧杯、玻璃棒、漏斗,玻璃棒在过滤中的作用是引流.过滤操作中滤纸有多种折法,为了加快过滤速率,如图乙,你选择折法是A.

下表是检测报告的一部分.
| 项目 | 标准 |
| 感官指标 | 无色、无异味、无异臭 |
| 化学指标 | pH7.5,铜<1.0mg•L-1,铁<0.3mg•L-1,氟化物<1.0mg•L-1,游离氯≥0.3mg•L-1等 |
(3)化学指标中的铜、铁是指元素(填“元素”或“单质”),水中的“铁”以铁离子形式存在,铁离子的符号是Fe3+.
(4)“pH”指标表示酸碱性:若pH=7,表示中性;pH<7,表示酸性;pH>7,表示碱性.检测报告表明瘦西湖水呈碱性(填“酸性”“碱性”或“中性”).
(5)实验室用瘦西湖水制取蒸馏水的方法是D.
A.吸附 B.沉淀 C.过滤 D.蒸馏
(6)如图丙是一种家用环保型消毒液发生器,其中发生的主要反应是氯化钠和水在通电条件下反应生成氢氧化钠(NaOH)和两种气体单质(其中一种是最轻的气体),该反应的化学式表达式为2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑;从能量变化角度看,该反应将电能转化为化学能.
7.下列变化属于分解反应的是( )
| A. | 水$\stackrel{通电}{→}$氧气+氢气 | B. | 氧气+氢气$\stackrel{点燃}{→}$水 | ||
| C. | 汞+氧气$\stackrel{加热}{→}$氧化汞 | D. | 食盐水$\stackrel{蒸发}{→}$水+食盐 |
17.大型客机C919是中国自主设计、研制的第二种国产新型客机,预计2015年底上市.其部分机身采用了新型的铝锂合金,这种材料具有较高的强度和适宜的延展性.铝锂合金中的铝(Al)元素与锂(Li)元素的本质区别是( )
| A. | 原子的质量不同 | B. | 原子的电子数不同 | ||
| C. | 原子的质子数不同 | D. | 原子的中子数不同 |
3.小明将家中清洗伤口用的消毒液--“双氧水”拿到学校的实验室,在老师的指导下和同学们一起做了如下实验.
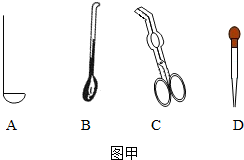
【实验准备】如图甲所示,取用少量双氧水的仪器是D(选填编号).
【实验1】小明欲证明该双氧水是否失效.
(1)实验过程(如图1)
①在试管中加入5mL“双氧水”,把带火星的木条伸入试管中,发现木条未复燃;
②用酒精灯给上述试管加热,液体中有气泡产生,把带火星的木条伸入试管中,发现木条仍未复燃;
③如右图装置进行操作,带火星的木条复燃,水槽中冰水所起的作用是使氧气中的水蒸气冷凝.
(2)实验结论:双氧水没有失效.
【实验2】氧化铜(CuO)能否催化“双氧水”分解.
【猜想】
Ⅰ.CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ.CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ.CuO是反应催化剂,反应前后质量和化学性质不变.
【实验】用天平称量0.2gCuO,取5mL的过氧化氢溶液于试管中,进行如下实验(如图2):
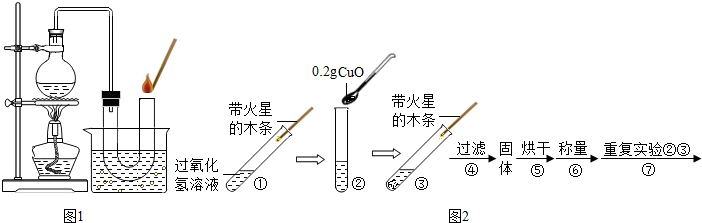
(3)完成下表:
(4)步骤③结束后,用手接触试管底部,感觉烫手.说明“双氧水”分解的化学反应放热(选填“放热”或“吸热”).
(5)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗(带滤纸)、烧杯、玻璃棒.
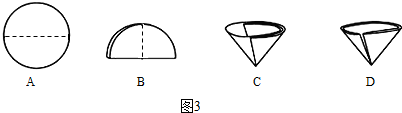
(6)操作④中需要将圆形滤纸折叠处理,图3中不该出现的情形是D(填序号).
(7)过氧化氢(H2O2)能被CuO催化分解放出O2,该反应的表达式为2H2O2$\frac{\underline{\;CuO\;}}{\;}$2H2O+O2↑.
【实验准备】如图甲所示,取用少量双氧水的仪器是D(选填编号).

【实验1】小明欲证明该双氧水是否失效.
(1)实验过程(如图1)
①在试管中加入5mL“双氧水”,把带火星的木条伸入试管中,发现木条未复燃;
②用酒精灯给上述试管加热,液体中有气泡产生,把带火星的木条伸入试管中,发现木条仍未复燃;
③如右图装置进行操作,带火星的木条复燃,水槽中冰水所起的作用是使氧气中的水蒸气冷凝.
(2)实验结论:双氧水没有失效.
【实验2】氧化铜(CuO)能否催化“双氧水”分解.
【猜想】
Ⅰ.CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ.CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ.CuO是反应催化剂,反应前后质量和化学性质不变.
【实验】用天平称量0.2gCuO,取5mL的过氧化氢溶液于试管中,进行如下实验(如图2):

(3)完成下表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 溶液中有气泡冒出, 带火星的木条复燃. | 仍为0.2g (氧化铜质量不变) | 溶液中有气泡放出, 使带火星木条复燃. | 猜想Ⅰ、Ⅱ不成立,猜想Ⅲ成立. |
(5)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗(带滤纸)、烧杯、玻璃棒.
(6)操作④中需要将圆形滤纸折叠处理,图3中不该出现的情形是D(填序号).

(7)过氧化氢(H2O2)能被CuO催化分解放出O2,该反应的表达式为2H2O2$\frac{\underline{\;CuO\;}}{\;}$2H2O+O2↑.
4.T℃时,在两只各盛有50克水的烧杯中,分别加入30克氯化钠和蔗糖固体,搅拌使其充分溶解,结果如图所示.下列说法正确的是( )


| A. | 两烧杯中的溶液质量相等 | |
| B. | 继续搅拌最终可使氯化钠溶解 | |
| C. | 氯化钠溶液一定是该温度下的饱和溶液 | |
| D. | 蔗糖溶液一定是该温度下的不饱和溶液 |
