题目内容
【题目】如图为氢氧化钙的溶解度曲线,下列说法不正确的是( )
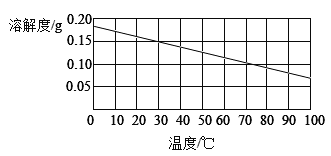
A.氢氧化钙的溶解度随温度的升高而减小
B.30℃时,100g水中最多溶解0.15g氢氧化钙
C.30℃恰好饱和的石灰水升温到50℃,溶质的质量分数不变
D.70℃时,饱和石灰水中溶剂和溶质的质量比为1000:1
【答案】C
【解析】
A、由图可知,氢氧化钙的溶解度随温度的升高而减小,说法正确,不符合题意;
B、由图可知,30℃时,氢氧化钙的溶解度是0.15g,即该温度下,100g水中最多溶解0.15g氢氧化钙,说法正确,不符合题意;
C、由图可知,氢氧化钙的溶解度随温度的升高而减小,30℃时,恰好饱和的石灰水升温到50℃,升温后溶解度变小,有溶质析出,溶质质量分数变小,说法不正确,符合题意;
D、由图可知,70℃时,氢氧化钙的溶解度是0.1g,故该温度下,饱和石灰水中溶剂和溶质的质量比为:100g:0.1g=1000:1,说法正确,不符合题意。
故选C。

 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案【题目】糕点疏松剂的主要成分有碳酸氢钠(白色固体)。某化学兴趣小组的同学对碳酸氢钠的性质进行了探究。
实验一:探究碳酸氢钠溶液的酸碱性
测量碳酸氢钠溶液的pH,约为10,由此可知碳酸氢钠溶液呈_____性。
实验二:探究碳酸氢钠的热稳定性
(查阅资料)碳酸氢钠受热容易分解,生成水、二氧化碳气体和一种常见的固体物质。
(进行实验)取一定质量的碳酸氢钠放到铜片上加热。如图所示。

(1)加热一段时间后,观察到烧杯内壁有水珠。实验装置中用到了铜片,主要利用了铜的_____性。
(2)在(1)实验的基础上,如何证明烧杯中还有二氧化碳生成_____(请简述实验方案)。
(3)为了确定实验(1)充分加热后的固体产物的成分,该小组同学又进行实验探究。
(提出假设)猜想①可能是Na2CO3;猜想②可能是NaOH
(设计实验)甲同学方案:取少量充分加热后的固体产物于试管中,加适量水配成溶液,滴加几滴酚酞试液,溶液变红,证明猜想②成立。乙同学认为甲方案不合理,他的理由是_____。
乙同学方案:
实验操作 | 实验现象 | 结论 |
取少量充分加热后的固体产物于试管中,_____ | _____ | 假设①成立,假设②不成立 |
(实验结论)NaHCO3受热分解的化学方程式为_____。