题目内容
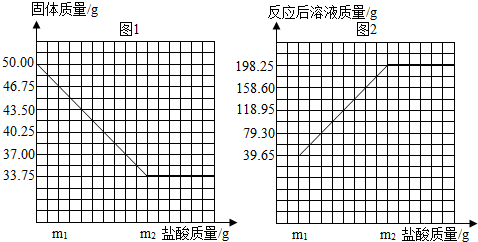
普通黄铜由铜和锌组成,广泛用于制造板材、管材等,也用于铸造机械零件等.为了测定某黄铜样品中铜的含量,设计了如下实验方案.取50.00 g黄铜样品,加入一种未知浓度的稀盐酸.有关实验数据如下图.


(1)样品完全反应产生H2的质量________.
(2)图中m与n的关系是m________n(填“>”、“<”或“﹦”).
(3)黄铜样品中铜的质量分数是多少(写出计算过程,保留小数点后一位).
(4)某同学根据图中数据计算盐酸的溶质质量分数为:
![]() ×100%=
×100%=![]() ×100=10.03%
×100=10.03%
请分析该同学的计算结果是否正确,如不正确指出错误的原因:________.
答案:
解析:
解析:
|
(1)0.5 (2)﹦ (3)67.5%(3分) (4)盐酸的质量:反应后溶液减去锌元素质量外,没有加上氢气中氢元素的质量.(2分) |

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目




 ×100%=
×100%= ×100%=10.03%请分析该同学的计算结果是否正确,如不正确指出错误的原因:______.
×100%=10.03%请分析该同学的计算结果是否正确,如不正确指出错误的原因:______.