题目内容
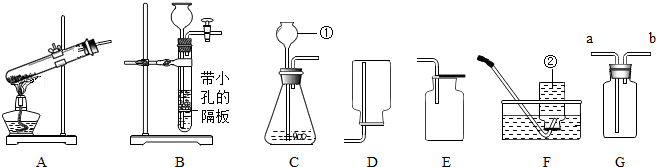
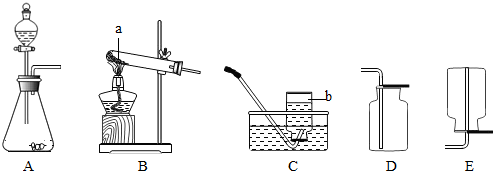
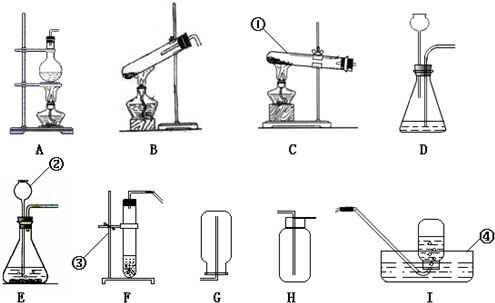
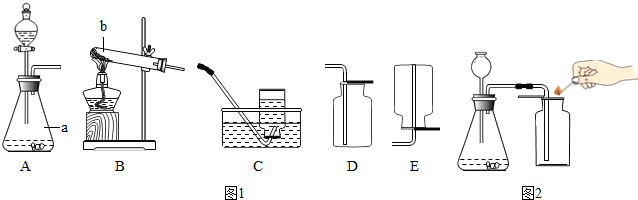
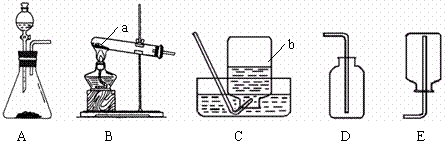
通过近一个学期的化学学习,你已经掌握了实验室制取气体的有关规律,以下是老师提供的一些实验装置.请结合下图回答问题:
(1)写出图中标号的仪器名称:a______b______.
(2)①写出实验室用B装置制取氧气的化学方程式______△ 2KCl+3O2↑
【答案】分析:(1)根据常见仪器及用途,写出图中指定仪器的名称;
(2)①根据B装置的特点适合于“固+固加热型”的反应,且试管口无棉花,故实验室制氧气选取的药品是氯酸钾与二氧化锰的混合物,再根据反应原理写出其反应的化学方程式;
②收集较纯净氧气时,采用排水集气法最好,当导管口气泡连续均匀的冒出时,才能收集;
③考虑影响化学反应速率的原因主要有哪些,并根据这些原因分析解答;
(3)实验组装与准备:
①根据制操作的一般方法,加入药品前,要检查装置的气密性;
②分析装置中可能存在的问题,解释造成意外现象的原因;
计算过程:
利用反应的化学方程式,以及二氧化碳的质量,计算所需碳酸钙的质量,并进而求出鸡蛋壳的质量;
实验反思与评价:
①根据题中所给信息并进行分析,判断该假设对实验结果的影响;
②将鸡蛋壳捣碎的目的是增大反应物的接触面积,使反应充分进行.
解答:解:(1)熟记常用仪器的名称可知:a为试管;b为集气瓶;
故答案为:铁架台;集气瓶;
(2)①由B装置的特点,需要加热且无棉花,可知实验室制氧气选取的药品是氯酸钾与二氧化锰的混合物,其反应的化学方程式为:2KClO3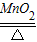 2KCl+3O2↑;
2KCl+3O2↑;
故答案为:2KClO3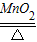 2KCl+3O2↑;
2KCl+3O2↑;
②用C装置收集较纯净氧气时,要等观察到连续均匀放出气泡现象时,再开始收集,防止收集的气体不纯,混有空气;
故选C;
③如果反应剧烈,集气瓶越小越危险,越加热反应越剧烈,而减慢液体滴加的速度可以减缓反应速度;
故选A.
(3)①装置连接完毕,应进行装置气密性的检查,然后再加入药品;
故答案为:检查装置气密性;
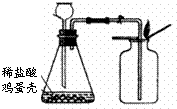
②木条没熄灭说明可能没有收集到气体,观察装置图,长颈漏斗没伸入液面以下,生成的气体从长颈漏斗逸出,所以未收集到气体;
故答案为:长颈漏斗下端管口未伸入液面以下,气体从长颈漏斗逸出;
实验设计:
二氧化碳的质量 2.2Lⅹ2.0g/L=4.4g
解:设该鸡蛋壳中碳酸钙的质量为x
CaCO3+2HC═CaCl2+CO2↑+H2O
100 44
x 4.4 g
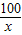 =
=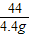
x=10 g
10g÷(1-20%)=12.5g
答:鸡蛋壳的质量为12.5 g
实验反思与评价:
①实验中,如有部分生成的二氧化碳气体因溶解于水而没有全部逸出,则使测量的二氧化碳体积减少,从而使气体的质量减少,计算出的碳酸钙的质量减少,对应的鸡蛋壳的质量减少,造成计算结果与实际值相比偏小;
故答案为:偏小;
②将鸡蛋壳捣碎的目的是增大反应物的接触面积,使反应充分进行;
故答案为:增大反应物的接触面积,使反应充分进行.
点评:本题考查的知识比较全面,既考查了实验室制取氧气的仪器名称、由装置特点选择反应药品及其反应的化学方程式书写等基础知识,还考查了根据方程式的计算、实验评价等内容,能综合考查学生对知识的掌握和应用能力.
(2)①根据B装置的特点适合于“固+固加热型”的反应,且试管口无棉花,故实验室制氧气选取的药品是氯酸钾与二氧化锰的混合物,再根据反应原理写出其反应的化学方程式;
②收集较纯净氧气时,采用排水集气法最好,当导管口气泡连续均匀的冒出时,才能收集;
③考虑影响化学反应速率的原因主要有哪些,并根据这些原因分析解答;
(3)实验组装与准备:
①根据制操作的一般方法,加入药品前,要检查装置的气密性;
②分析装置中可能存在的问题,解释造成意外现象的原因;
计算过程:
利用反应的化学方程式,以及二氧化碳的质量,计算所需碳酸钙的质量,并进而求出鸡蛋壳的质量;
实验反思与评价:
①根据题中所给信息并进行分析,判断该假设对实验结果的影响;
②将鸡蛋壳捣碎的目的是增大反应物的接触面积,使反应充分进行.
解答:解:(1)熟记常用仪器的名称可知:a为试管;b为集气瓶;
故答案为:铁架台;集气瓶;
(2)①由B装置的特点,需要加热且无棉花,可知实验室制氧气选取的药品是氯酸钾与二氧化锰的混合物,其反应的化学方程式为:2KClO3
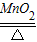 2KCl+3O2↑;
2KCl+3O2↑;故答案为:2KClO3
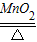 2KCl+3O2↑;
2KCl+3O2↑;②用C装置收集较纯净氧气时,要等观察到连续均匀放出气泡现象时,再开始收集,防止收集的气体不纯,混有空气;
故选C;
③如果反应剧烈,集气瓶越小越危险,越加热反应越剧烈,而减慢液体滴加的速度可以减缓反应速度;
故选A.
(3)①装置连接完毕,应进行装置气密性的检查,然后再加入药品;
故答案为:检查装置气密性;
②木条没熄灭说明可能没有收集到气体,观察装置图,长颈漏斗没伸入液面以下,生成的气体从长颈漏斗逸出,所以未收集到气体;
故答案为:长颈漏斗下端管口未伸入液面以下,气体从长颈漏斗逸出;
实验设计:
二氧化碳的质量 2.2Lⅹ2.0g/L=4.4g
解:设该鸡蛋壳中碳酸钙的质量为x
CaCO3+2HC═CaCl2+CO2↑+H2O
100 44
x 4.4 g
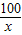 =
=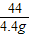
x=10 g
10g÷(1-20%)=12.5g
答:鸡蛋壳的质量为12.5 g
实验反思与评价:
①实验中,如有部分生成的二氧化碳气体因溶解于水而没有全部逸出,则使测量的二氧化碳体积减少,从而使气体的质量减少,计算出的碳酸钙的质量减少,对应的鸡蛋壳的质量减少,造成计算结果与实际值相比偏小;
故答案为:偏小;
②将鸡蛋壳捣碎的目的是增大反应物的接触面积,使反应充分进行;
故答案为:增大反应物的接触面积,使反应充分进行.
点评:本题考查的知识比较全面,既考查了实验室制取氧气的仪器名称、由装置特点选择反应药品及其反应的化学方程式书写等基础知识,还考查了根据方程式的计算、实验评价等内容,能综合考查学生对知识的掌握和应用能力.

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目