题目内容
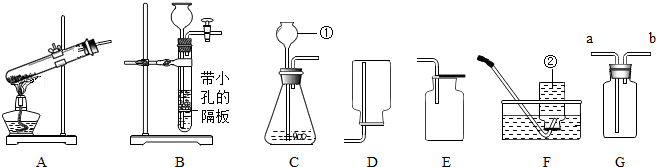
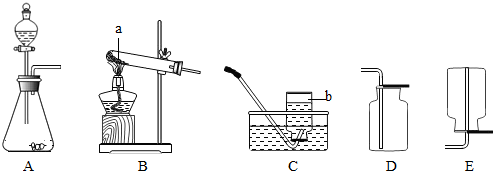
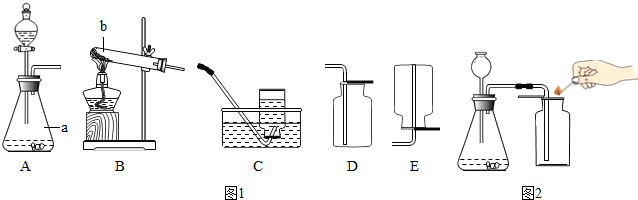
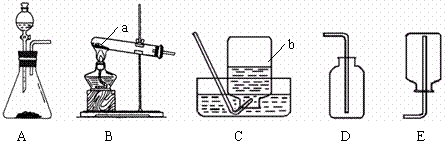
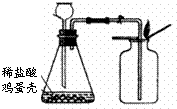
通过近一个学期的化学学习,你已经掌握了实验室制取气体的有关规律,请结合下图回答问题:
(1)写出图中标号仪器的名称①
(2)用加热氯酸钾的方法制取氧气,应选用的发生装置是
(3)实验室利用
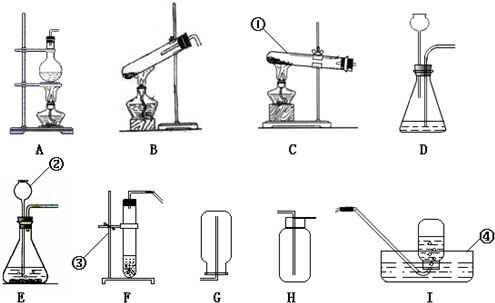
(1)写出图中标号仪器的名称①
试管
试管
; ②长颈漏斗
长颈漏斗
;③铁架台
铁架台
;④水槽
水槽
.(2)用加热氯酸钾的方法制取氧气,应选用的发生装置是
C
C
(填字母,下同).反应的化学方程式为2KClO3
2KCl+3O2↑
| ||
| △ |
2KClO3
2KCl+3O2↑
.如果改用高锰酸钾制取氧气,应该做何变动?
| ||
| △ |
在试管口放一团棉花
在试管口放一团棉花
,原因是防止加热时高锰酸钾粉末进入导管
防止加热时高锰酸钾粉末进入导管
.(3)实验室利用
大理石或石灰石
大理石或石灰石
和稀盐酸
稀盐酸
反应制取二氧化碳,应选用的发生装置是E或F
E或F
;收集装置是H
H
,在实验室制取氢气中,能否用此装置收集氢气否
否
(填“能”或“否”).请写出实验室制取氢气的化学方程式:Zn+H2SO4=ZnSO4+H2↑
Zn+H2SO4=ZnSO4+H2↑
.
分析:(1)据常用仪器回答;
(2)加热氯酸钾属于固体加热型,故选 发生装置BC,并结合加热固体的方法分析解答;结合反应原理书写方程式,若用高锰酸钾制取,须在试管口放一些棉花,防止加热时高锰酸钾粉末进入导管;
(3)据实验室制取二氧化碳的药品、反应原理、反应物的状态和反应条件选择发生装置,据气体的密度和溶解性选择收集装置,氢气的密度比空气小,所以不能用向上排空气法收集,锌和硫酸反应生成硫酸锌和氢气,据此分析解答.
(2)加热氯酸钾属于固体加热型,故选 发生装置BC,并结合加热固体的方法分析解答;结合反应原理书写方程式,若用高锰酸钾制取,须在试管口放一些棉花,防止加热时高锰酸钾粉末进入导管;
(3)据实验室制取二氧化碳的药品、反应原理、反应物的状态和反应条件选择发生装置,据气体的密度和溶解性选择收集装置,氢气的密度比空气小,所以不能用向上排空气法收集,锌和硫酸反应生成硫酸锌和氢气,据此分析解答.
解答:解:(1)标号仪器分别是:试管、长颈漏斗、铁架台、水槽;
(2)加热氯酸钾属于固体加热型,故选 发生装置BC,给试管内的固体加热,试管口要低于试管底部,防止冷凝水倒流引起试管炸裂,且试管内导管不能伸的太长,不利于气体导出,所以用C装置,反应的方程式是:2KClO3
2KCl+3O2↑;如果改用高锰酸钾制取氧气,须在试管口放一些棉花,防止加热时高锰酸钾粉末进入导管;
(3)实验室制取二氧化碳用大理石或石灰石和稀盐酸反应,属于固液常温型,故选发生装置E、F,不能用D,因为长颈漏斗下端未伸入液面以下,气体会从长颈漏斗逸出;二氧化碳密度比空气大且能溶于水,所以用向上排空气法收集;氢气的密度比空气小,所以不能用向上排空气法收集,实验室常用锌和硫酸反应生成硫酸锌和氢气,反应的方程式是:Zn+H2SO4=ZnSO4+H2↑;
故答案为:(1)试管;长颈漏斗;铁架台;水槽;
(2)C;2KClO3
2KCl+3O2↑;在试管口放一团棉花;防止加热时高锰酸钾粉末进入导管;
(3)大理石或石灰石;稀盐酸;E或F;H;否;Zn+H2SO4=ZnSO4+H2↑.
(2)加热氯酸钾属于固体加热型,故选 发生装置BC,给试管内的固体加热,试管口要低于试管底部,防止冷凝水倒流引起试管炸裂,且试管内导管不能伸的太长,不利于气体导出,所以用C装置,反应的方程式是:2KClO3
| ||
| △ |
(3)实验室制取二氧化碳用大理石或石灰石和稀盐酸反应,属于固液常温型,故选发生装置E、F,不能用D,因为长颈漏斗下端未伸入液面以下,气体会从长颈漏斗逸出;二氧化碳密度比空气大且能溶于水,所以用向上排空气法收集;氢气的密度比空气小,所以不能用向上排空气法收集,实验室常用锌和硫酸反应生成硫酸锌和氢气,反应的方程式是:Zn+H2SO4=ZnSO4+H2↑;
故答案为:(1)试管;长颈漏斗;铁架台;水槽;
(2)C;2KClO3
| ||
| △ |
(3)大理石或石灰石;稀盐酸;E或F;H;否;Zn+H2SO4=ZnSO4+H2↑.
点评:了解并掌握实验室利用高锰酸钾制取氧气、氢气的反应原理、实验注意事项、装置选取方法等知识,并能据题意灵活解答问题.

练习册系列答案
相关题目