题目内容
以下是初中化学的一些基本实验: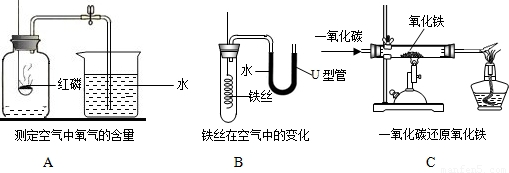
(1)A中可燃物应过量的原因是______;
(2)一段时间后,B中U形管中液面变化情况为______;
(3)C中硬质玻璃管内发生反应的实验现象是______,化学方程式为______ 2Fe+3CO2
【答案】分析:(1)A实验是实验室测定空气中氧气的含量,红磷的作用为消耗空气中的氧气,造成气体体积减少,压强减小;
(2)铁丝生锈是铁与氧气、水蒸气发生的复杂的化学反应;
(3)一氧化碳和红色的氧化铁反应生成黑色的铁和二氧化碳,通入的一氧化碳不能完全反应,所以酒精灯的作用就是点燃一氧化碳,消除有害气体;
(4)一氧化碳和红色的氧化铁反应生成二氧化碳,二氧化碳不支持燃烧;
解答:解:(1)A实验测定空气中氧气的含量,故应使红磷足量充分消耗氧气,故答案为:确保集气瓶中的氧气完全反应
(2)B实验铁丝生锈消耗空气中的氧气和水蒸气,管内外形成气压差,故U型管中液面左高右低,故答案为:铁丝生锈,U型管中液面左高右低
(3)一氧化碳和红色的氧化铁反应生成黑色的铁和二氧化碳,反应现象为:红色的粉末变成黑色的粉末,反应的方程式为:Fe2O3+3CO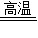 2Fe+3CO2,由于通入的一氧化碳不能完全反应,所以酒精灯的作用就是点燃一氧化碳,消除有害气体. 故答案为:红色的粉末变成黑色;Fe2O3+3CO
2Fe+3CO2,由于通入的一氧化碳不能完全反应,所以酒精灯的作用就是点燃一氧化碳,消除有害气体. 故答案为:红色的粉末变成黑色;Fe2O3+3CO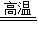 2Fe+3CO2;点燃未反应的CO,防止其污染空气
2Fe+3CO2;点燃未反应的CO,防止其污染空气
(4)分析以上实验,C实验由于一氧化碳和红色的氧化铁反应生成二氧化碳,二氧化碳不支持燃烧,在尾气点燃少量剩余的一氧化碳时不容易点燃,所以应先把尾气通入的氢氧化钠溶液中除去,再点燃除去一氧化碳.故答案为:C;先把尾气通入的氢氧化钠溶液后再点燃
点评:此题考查了解,探究测定空气中氧气含量的方法,金属生锈的条件,以及一氧化碳还原氧化铁的实验等注意事项,能开拓学生的思维能力.
(2)铁丝生锈是铁与氧气、水蒸气发生的复杂的化学反应;
(3)一氧化碳和红色的氧化铁反应生成黑色的铁和二氧化碳,通入的一氧化碳不能完全反应,所以酒精灯的作用就是点燃一氧化碳,消除有害气体;
(4)一氧化碳和红色的氧化铁反应生成二氧化碳,二氧化碳不支持燃烧;
解答:解:(1)A实验测定空气中氧气的含量,故应使红磷足量充分消耗氧气,故答案为:确保集气瓶中的氧气完全反应
(2)B实验铁丝生锈消耗空气中的氧气和水蒸气,管内外形成气压差,故U型管中液面左高右低,故答案为:铁丝生锈,U型管中液面左高右低
(3)一氧化碳和红色的氧化铁反应生成黑色的铁和二氧化碳,反应现象为:红色的粉末变成黑色的粉末,反应的方程式为:Fe2O3+3CO
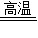 2Fe+3CO2,由于通入的一氧化碳不能完全反应,所以酒精灯的作用就是点燃一氧化碳,消除有害气体. 故答案为:红色的粉末变成黑色;Fe2O3+3CO
2Fe+3CO2,由于通入的一氧化碳不能完全反应,所以酒精灯的作用就是点燃一氧化碳,消除有害气体. 故答案为:红色的粉末变成黑色;Fe2O3+3CO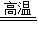 2Fe+3CO2;点燃未反应的CO,防止其污染空气
2Fe+3CO2;点燃未反应的CO,防止其污染空气(4)分析以上实验,C实验由于一氧化碳和红色的氧化铁反应生成二氧化碳,二氧化碳不支持燃烧,在尾气点燃少量剩余的一氧化碳时不容易点燃,所以应先把尾气通入的氢氧化钠溶液中除去,再点燃除去一氧化碳.故答案为:C;先把尾气通入的氢氧化钠溶液后再点燃
点评:此题考查了解,探究测定空气中氧气含量的方法,金属生锈的条件,以及一氧化碳还原氧化铁的实验等注意事项,能开拓学生的思维能力.

练习册系列答案
相关题目



 (2013?宝坻区二模)以下是初中化学的一些基本实验:
(2013?宝坻区二模)以下是初中化学的一些基本实验: