题目内容
下列推理中说法中,正确的是( )
①饱和溶液不能继续溶解某种溶质,则饱和溶液也不能继续溶解其他溶质;②Na2MoO4中钼(Mo)元素的化合价是+6价;③盐是由金属离子和酸根离子组成,NH4NO3中没有金属离子,不属于盐;④化学变化中,原子的种类和个数不变;⑤带电的微粒都称为离子;⑥NaOH溶液中的OH﹣能与酸反应,则KOH溶液中的OH﹣也能与酸反应.
|
| A. | ①②④ | B. | ②④⑥ | C. | ①③⑤ | D. | ③⑤⑥ |
考点:
饱和溶液和不饱和溶液;碱的化学性质;常见的氧化物、酸、碱和盐的判别;原子和离子的相互转化;有关元素化合价的计算;化学反应的实质.
专题:
化学式的计算;物质的微观构成与物质的宏观组成;溶液、浊液与溶解度;物质的分类;常见的碱 碱的通性.
分析:
①根据饱和溶液的定义判断.
②根据化合物中化合价代数和为零的原则来计算解答;
③根据盐的定义判断;
④根据化学变化中,原子的种类和个数不变来分析;
⑤根据带电微粒有质子、电子、离子等来判断;
⑥根据碱溶液的化学性质相似的原因判断.
解答:
解:①某溶质的饱和溶液不能再继续溶解该溶质,但还可能再溶解其它的物质,所以错误.
②设钼(Mo)元素的化合价为x,钠的为+1价,氧的为﹣2价,则 (+1)×2+x+(﹣2)×4=0,x=+6;正确;
③盐是指由金属离子(或铵根离子)与酸根离子构成的化合物,NH4NO3中没有金属离子,但有铵根离子,属于盐类,所以错误.
④化学变化中,原子的种类和个数不变,正确;
⑤带电的微粒不一定都为离子,还可能是质子、电子;错误;
⑥碱溶液之所以化学性质相似,是因为它们的溶液中都含有氢氧根离子,氢氧化钾溶液中也有OH﹣,故和所有的碱溶液一样,也能与酸反应,所以正确.
答案:B.
点评:
酸、碱、盐是初中化学最重点的部分,在中考中占有重要地位,特别是对基本概念和理论的理解和运用,透彻理解概念是解题的必要前提.

汤姆森和卢瑟福都对现代原子结构理论做出了巨大贡献.下列关于原子结构的论述中,不属于他们两人共同观点的是( )
|
| A. | 原子很小,但可以分 |
|
| B. | 原子是构成物质的基本粒子 |
|
| C. | 原子的电子带负电荷 |
|
| D. | 原子由原子核和核外电子构成 |
在日常生活中,下列说法正确的是( )
|
| A. | 用炉具清洁剂清洗家中的排油烟机,利用的是清洁剂的乳化作用 |
|
| B. | 包装食品的聚乙烯塑料袋可用加热的方法封口 |
|
| C. | 冬天室内用煤炉取暖,为防止煤气中毒,在煤炉上放一盆水 |
|
| D. | 图书档案着火,最好用干粉灭火器灭火 |
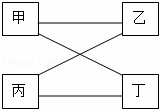
如图所示,处于连线两端的物质,在一定的条件下都能发生化学反应的物质组别是( )
| 甲 | 乙 | 丙 | 丁 | |
| A | C | O2 | H2SO4 | CuO |
| B | Fe | H2SO4 | CuCl2 | NaOH |
| C | NaOH | CO2 | KOH | CuCl2 |
| D | Na2SO4 | Ba(OH)2 | HCl | Ba(NO3)2 |
|
| A. | A | B. | B | C. | C | D. | D |
下列各组物质的溶液,需要加入其他试剂才能鉴别出来的是( )
|
| A. | NaOH NaCl KNO3 MgCl2 |
|
| B. | NaOH NaCl HCl FeCl3 |
|
| C. | Na2SO4 BaCl2 HCl K2CO3 |
|
| D. | Na2CO3 H2SO4 HCl Ba(NO3)2 |


 红色固体J”的转化,物质I必领满足的条件是 .
红色固体J”的转化,物质I必领满足的条件是 .