题目内容
15.“粗盐提纯”指除去NaCl中的泥沙和MgCl2、CaCl2、Na2SO4等杂质,工业提纯粗盐的工艺流程如图所示.请回答: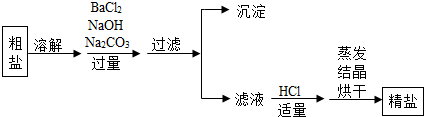
(1)在溶解、过滤、蒸发的过程中均用到了同一玻璃仪器,该仪器在蒸发时的作用是什么?
(2)用化学方程式表示加入碳酸钠的意义.
(3)有同学认为在滤液中即使过量加稀盐酸对提纯精盐也没有影响,为什么?
分析 (1)考虑仪器玻璃棒在蒸发时的作用;
(2)考虑碳酸钠的意义:除钡离子、钙离子;
(3)考虑加热时氯化氢气体逸散到空气中.
解答 解:(1)在溶解、过滤、蒸发的过程中均用到了仪器玻璃棒,在蒸发时的作用为搅拌,防止局部过热液滴飞溅;
(2)因为碳酸钠的意义:除钡离子、钙离子,故其化学方程式为Na2CO3+BaCl2=BaCO3↓+2NaCl;Na2CO3+CaCl2=CaCO3↓+2NaCl;
(3)在滤液中即使过量加稀盐酸对提纯精盐也没有影响,因为加热时氯化氢气体逸散到空气中.
故答案为:
(1)搅拌,防止局部过热液滴飞溅;(2)Na2CO3+BaCl2=BaCO3↓+2NaCl; Na2CO3+CaCl2=CaCO3↓+2NaCl;(3)因为在加热时氯化氢气体逸散到空气中去了.
点评 粗盐提纯是经常考查的内容,其中要涉及到化学方程式的书写、过滤操作、杂质的除去等内容,需要同学们对此内容了然于心.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
5.根据“绿色化学”的要求,下列做法不合理的是( )
| A. | 改进造纸厂生产工艺,减少废水排放 | |
| B. | 农业生产时用化肥代替农家肥料,提高作物产量 | |
| C. | 优化能源结构,开发新能源以减轻对化石燃料的依赖 | |
| D. | 对金属产品回收利用,减少矿石开采 |
6.硫代硫酸钠(Na2S2O5)是一种重要的化工产品,其中硫元素的化合价是( )
| A. | +4 | B. | +6 | C. | -4 | D. | -6 |
3.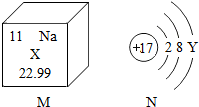 如图为元素周期表中的一格和某离子结构示意图,下列说法错误的是( )
如图为元素周期表中的一格和某离子结构示意图,下列说法错误的是( )
 如图为元素周期表中的一格和某离子结构示意图,下列说法错误的是( )
如图为元素周期表中的一格和某离子结构示意图,下列说法错误的是( )| A. | M原子核内有11个质子 | B. | 根据题意Y的值应为7 | ||
| C. | M和N可形成离子化合物 | D. | M易失去电子形成Na+ |
7.下列实验方法中,不能达到实验目的是( )
| A | 用过滤的方法除去黄河水中的泥沙 |
| B | 用水鉴别硫酸铜固体和氢氧化钠固体 |
| C | 用BaCl2溶液中除去NaCl溶液中的Na2CO3杂质 |
| D | 用燃着的木条鉴别二氧化碳和氮气 |
| A. | A | B. | B | C. | C | D. | D |
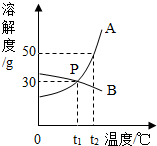 如图是A、B两种物质的溶解度曲线,右图是A、B的溶解度曲线.P点意义为t1℃时AB的溶解度相等;把t2℃时150gA的饱和溶液稀释为20%,需加水100gg.
如图是A、B两种物质的溶解度曲线,右图是A、B的溶解度曲线.P点意义为t1℃时AB的溶解度相等;把t2℃时150gA的饱和溶液稀释为20%,需加水100gg.