题目内容
比较上述实验,试说明酸雨可能对环境造成什么样的破坏,应采取怎样的防止和保护措施.
答案:略
解析:
解析:
|
讨论:酸雨对环境造成的破坏:①对人体健康的直接危害,硫酸雾和硫酸盐雾的毒性比二氧化硫大得多,可以侵入肺的深部组织,引起肺水肿等疾病而使人死亡;②引起河流、湖泊的水体酸化,严重影响水生动植物的生长;③破坏土壤、植被、森林;④腐蚀金属、油漆、皮革、纺织品及建筑材料等;⑤渗入地下,可能引起地下水酸化,酸化的水中铝、铜、锌的含量比中性地下水中高很多倍. 防止和保护措施:①尽量少用含硫燃料;②含硫燃料脱硫后再使用,③除去烟道气中的有害气体再排放;④开发新能源. |

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案
相关题目
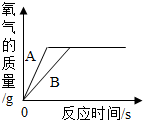 化学兴趣小组同学对“金属活动性顺序”从内容、规律以及应用等方面进行了总结,请按要求填空:
化学兴趣小组同学对“金属活动性顺序”从内容、规律以及应用等方面进行了总结,请按要求填空: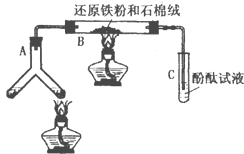 某版本的化学教材中安排了如图所示“合成氨”的演示实验(夹持仪器均已省略).在Y形管的一侧用Zn粒和稀H2SO4反应制取H2,另一侧用NaNO2固体和饱和NH4Cl溶液反应制取N2,N2和H2混合通过还原铁粉来合成NH3,再将产生的气体通入酚酞试液中,若酚酞试液变红,即说明产生了氨气.某课外活动小组通过查阅资料和多次实验,得到了如下信息:
某版本的化学教材中安排了如图所示“合成氨”的演示实验(夹持仪器均已省略).在Y形管的一侧用Zn粒和稀H2SO4反应制取H2,另一侧用NaNO2固体和饱和NH4Cl溶液反应制取N2,N2和H2混合通过还原铁粉来合成NH3,再将产生的气体通入酚酞试液中,若酚酞试液变红,即说明产生了氨气.某课外活动小组通过查阅资料和多次实验,得到了如下信息: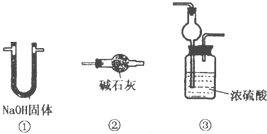

 (2007?宣武区二模)初中化学课学完以后,化学学习兴趣小组对“金属活动性顺序”从内容、规律以及应用等方面进行了总结.请你认真填写下面的空白内容:
(2007?宣武区二模)初中化学课学完以后,化学学习兴趣小组对“金属活动性顺序”从内容、规律以及应用等方面进行了总结.请你认真填写下面的空白内容: