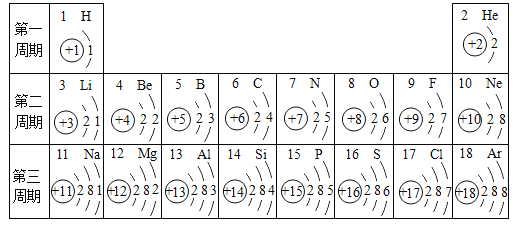
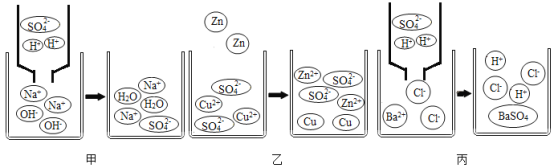
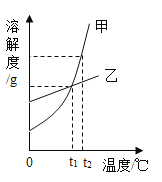
题目内容
【题目】氯化钠是重要的调味品,是舌尖上最不可缺少的味道,如图分别表示不同的化学反应,但均涉及到氯化钠。
(1)金属钠在氯气中燃烧产生大量白烟,图1是二者反应生成氯化钠的微观示意图,由图1可知,元素的化学性质主要与原子的_____(填字母序号)有密切的关系。
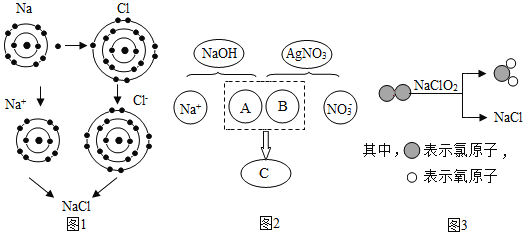
A 最外层电子数 B 核电荷数 C 电子层数 D 相对原子质量
(2)图2描述了氯化钠与硝酸银溶液的反应,试用A、B、C所代表的微粒符号表示该反应的_____。
(3)图3所示的四种物质中属于氧化物的是_____(写化学式),该反应的化学方程式为_____。
【答案】A ![]() ClO2
ClO2 ![]()
【解析】
(1)由图可知,当发生化学变化时,元素原子的最外层电子数发生了改变,故元素的化学性质与最外层电子数有密切的联系故选A;
(2)稀盐酸与硝酸银溶液反应属于复分解反应,根据反应实质可知,盐酸中的氯离子与硝酸银中的银离子结合成氯化银白色沉淀;该反应的实质是:Cl-+Ag+═AgCl↓;
(3)图3中![]() 是由两种元素组成且含有氧元素的化合物,属于氧化物,其化学式为ClO2,该反应的化学方程式为Cl2+2NaClO2═2ClO2+2NaCl;
是由两种元素组成且含有氧元素的化合物,属于氧化物,其化学式为ClO2,该反应的化学方程式为Cl2+2NaClO2═2ClO2+2NaCl;
故答案为:
(1)A;
(2)Cl-+Ag+═AgCl↓;
(3)ClO2;Cl2+2NaClO2═2ClO2+2NaCl。

 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案【题目】在研究酸和碱的化学性质时,某小组想证明稀硫酸和氢氧化钠混合后,虽然无明显现象,但确实发生了化学反应。试与他们一起完成实验方案的设计、实施和评价,并得出有关结论。
(1)探究稀硫酸和氢氧化钠溶液的反应:
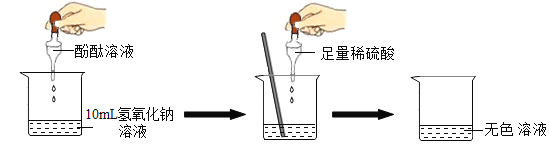
当滴入几滴酚酞溶液后,溶液由无色变为_________色。根据上述实验中颜色变化,可确定稀硫酸和氢氧化钠溶液发生了化学反应。
(2)探究上述稀硫酸和氢氧化钠溶液反应后烧杯中的硫酸是否过量:根据上述反应过程中溶液变成无色,不能确定稀硫酸是否过量。同学们又分别选取氯化钡溶液、紫色石蕊溶液设计实验方案,请你判断并(提示:Ba2+与SO42-可形成BaSO4白色沉淀)
实验方案 | 实验步骤 | 实验现象 | 实验结论 |
方案一 | 取样,滴入适量的氯化钡溶液 | 有白色沉淀生成 | 稀硫酸过量 |
方案二 | 取样,滴入几滴紫色石蕊溶液 | _________ | 稀硫酸过量 |
①上述设计的实验方案中,正确的方案是:__________。
②若请你再设计一个确定稀硫酸是否过量的实验方案,你会选用的药品是_______,实验现象及结论是_____________。
(3)成成同学认为稀硫酸和氢氧化钠溶液的反应没有明显现象,他提出可以对某些有明显现象产生的中和反应进行探究,如稀盐酸和氢氧化铝的反应,可观察到的现象为_________,说明中和反应已经发生,反应的化学方程式为_______________。。(提示:氢氧化铝是不溶于水的白色固体,化学式为Al(OH)3)。
(4)现取10g一定溶质质量分数的稀硫酸样品,将5%的NaOH溶液逐滴加入到样品中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化情况如图所示。计算恰好完全反应时所得溶液的溶质质量分数______。(结果精确到0.1%)
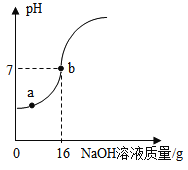
【题目】2018年5月18日我国第一艘国产航母试海成功,航母的许多电子元件使用了黄铜。为测定某黄铜(假设合金中仅含铜,锌)中铜的质量分数,兴趣小组同学称取20g黄铜粉末于烧杯中,将80g稀硫酸分四次加入,充分反应,测得实验数据如下表所示:
第一次 | 第二次 | 第三次 | 第四次 | |
加入稀硫酸的质量(g) | 20 | 20 | 20 | 20 |
烧杯中剩余物的质量(g) | 39.92 | 59.84 | 79.80 | 99.80 |
(1)黄铜粉末完全反应生成氢气的总质量为_______g。
(2)该黄铜中铜的质量分数为多少____________? (写出计算过程)
(3)第三次实验中溶质的种类为________________。
【题目】经过监测和治理,某省的土壤质量已经得到了很好的改善,但个别地区仍然存在盐碱地。某校化学兴趣小组的同学们为此开展了实践活动,他们采集了本地的土样,并对土样围绕两个问题进行探究。
(查阅资料)
①枸杞和合欢均可在轻度盐碱地中生存。
②盐碱地显碱性。
③该土样中的可溶性物质只含NaCl、CaCl2和Na2CO3。
(探究过程)
(1)甲组探究土样的酸碱度。具体操作是________,由此得出,该土样的pH>7。
(2)乙组探究土样的成分(如图所示)

向土样中加入足量的蒸馏水,发生反应的化学方程式为_____________。
同学们对溶液I中的溶质成分很感兴趣,作出如下猜想:
猜想一:只含NaCl;
猜想二:含NaCl、CaCl2;
猜想三:含NaCl、Na2CO3。
设计实验,继续探究。
1 | 验证猜想所用试剂 | 实验现象 | 实验结果 |
方案一 | AgNO3溶液和稀硝酸 | 有白色沉淀生成 | 猜想①正确 |
方案二 | ______ | 无明显现象 | 猜想②不正确 |
方案三 | 稀盐酸 | ________ | 猜想③正确 |
(反思与评价)
①通过交流,甲组认为乙组的方案一不太严谨,理由是___________。
②同学们对沉淀I中CaCO3的来源展开了热烈的讨论。一致认为CaCO3也可能来自土样本身。请解释土样中存在CaCO3的原因______________。
(总结与提升)改良该省的盐碱地,充分利用土地资源,造福人民,我们任重而道远。以下建议你认为正确的是____________。
a轻度盐碱地可以种植枸杞
b可以用熟石灰改良盐碱地
c盐碱地应避免施用碱性化肥
【题目】2019 年 9 月 29 日,我省于山西省农产品国际交易中心举办了中国(山西)特色农产 品交易博览会。某校化学兴趣小组的同学们参观博览会时,对农药波尔多液产生了浓厚的兴趣,于是同学们对其中的硫酸铜溶液开展了实践活动。
探究过程:
(1)甲组用无水硫酸铜固体配制 100g质量分数为 8%的 CuSO4 溶液

①需硫酸铜固体的质量为______。
②某同学按如图所示步骤依次操作,其中操作错误的步骤是______(填字母序号), 会导致配得的硫酸铜溶液溶质质量分数______(选填“偏大”、“偏小”、“不变”)。
③操作 E 中用玻璃棒搅拌,其目的是______。
(2) 为比较相同浓度的 CuSO4 溶液和 FeCl3 溶液对过 氧化氢分解的催化效果,乙组同学设计了如图所示的创新实验。

实验序号 | 5%H2O2 溶液体积/ml | 分液漏斗中所加物质 | 实验现象 |
实验一 | 50 | 无 | 无明显现象 |
实验二 | 50 | 5ml 8%CuSO4 溶液 | 注射器活塞向右移动 |
实验三 | 50 | 5ml 8%FeCl3 溶液 | 注射器活塞向右移动 |
设计实验
①实验前,应该先______ 。
②在乙组的探究实验中,“实验一”起的作用是______ 。
③为定量比较两者的催化效果,可测量生成等体积气体所需的______。
深入探究
④为了证明 CuSO4 溶液是该反应的催化剂,还需:a.验证______; b.验证______。
总结与提升:
同一物质可以有很多用途。当我们徜徉于化学的海洋时,会发现诸多的奇珍异宝 ,让 我们一起来探究物质更多的用途吧。