题目内容
把一块碳酸钙放入稀盐酸中,直到没有气体放出,且碳酸钙有剩余,所得溶液中溶质为 ,溶剂为 ;如果加入的碳酸钙没有剩余,则溶液中的溶质一定有 ,还可能有 .
考点:酸的化学性质
专题:常见的酸 酸的通性
分析:根据铁与稀盐酸反应生成氯化亚铁和氢气来解决问题.
解答:解:根据碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,如果碳酸钙有剩余,所得溶液中,溶质为氯化亚钙,溶剂为 水;如果碳酸钙没有剩余,可能稀盐酸过量,故则液体中的溶质一定有氯化钙,也可能还有 氯化氢
故答案为:CaCl2 H2O CaCl2 HCl
故答案为:CaCl2 H2O CaCl2 HCl
点评:本题主要考查了反应物的“过量”问题,熟记碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
下列有关实验现象的描述正确的是( )
| A、沾有浓硫酸的小木条逐渐变黑 |
| B、浓盐酸在空气中敞口放置出现白烟 |
| C、红磷在空气中燃烧产生大量白雾 |
| D、二氧化碳通入无色酚酞试液后溶液变色 |
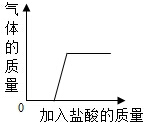 实验室有有一瓶敞口放置的氢氧化钠溶液,小刚取了适量的溶液于试管中,然后滴加足量的稀盐酸,产生的气体质量如图所示,请用化学方程式表示滴加盐酸过程中发生的反应
实验室有有一瓶敞口放置的氢氧化钠溶液,小刚取了适量的溶液于试管中,然后滴加足量的稀盐酸,产生的气体质量如图所示,请用化学方程式表示滴加盐酸过程中发生的反应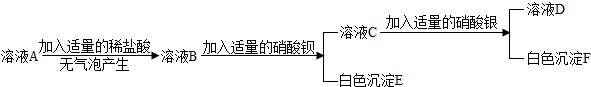
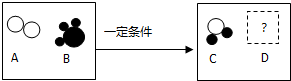
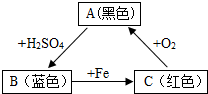 A、B、C三种物质(或溶液)可发生如图所示的转化.
A、B、C三种物质(或溶液)可发生如图所示的转化.