题目内容
某同学分别用1 g的铁屑、锌粒、镁片与足量的某酸反应以制取氢气.完全反应所需时间与当地的金属价格见下表:

你认为实验中一般不选用铁屑、镁片与酸反应制取氢气的主要原因是________.
答案:
解析:
解析:
|
一般不选Fe是因为反应速度太慢,难达实验要求,一般不选Mg是因为反应速度太快,不易控制,价格较贵. |

练习册系列答案
相关题目
某纺织厂为了除去棉麻原料中的非纤维素,可用一定溶质的质量分数的碳酸钠溶液煮沸棉麻原料.现需要80kg20%的碳酸钠溶液.
(1)若用碳酸钠固体和水配制上述溶液,需要碳酸钠的质量是 kg;水的质量是 kg.
(2)甲乙两组同学分别用不同的方案,探究所配得的溶液中碳酸钠的质量分数是否为20%,设计并完成了以下实验:
请用计算结果填空.
①甲组实验1中产生气体的质量是 g;
②依据甲乙两组的数据分别计算所配得的溶液中碳酸钠的质量分数;
甲: ; 乙: .(精确到0.1%)
测定结果与20%之间产生差异可能是实验原理、操作过程等因素引起的.
(1)若用碳酸钠固体和水配制上述溶液,需要碳酸钠的质量是
(2)甲乙两组同学分别用不同的方案,探究所配得的溶液中碳酸钠的质量分数是否为20%,设计并完成了以下实验:
| 甲组 | 乙组 | |||||||||||||||||
| 实验过程 | I.取质量是100g的三个烧杯,各盛20g所配得的碳酸钠溶液. II.向三个烧杯中分别放入溶质质量分数相同,但溶液质量不同的盐酸溶液; III.充分反应后再分别称量烧杯及剩余溶液; |
I.取质量是100g的一个烧杯,盛20g所配得的碳酸钠溶液. II.向三个烧杯中滴入溶质质量分数为20%的氯化钙溶液,直到不再产生沉淀为止,过滤、洗涤、晾干、称重; III.绘制加入氯化钙溶液与产生沉淀的质量关系如下图; | ||||||||||||||||
| 所得的数据或关系图 |
|
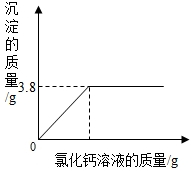 已知发生反应的化学方程式为: Na2CO3+CaCl2═CaCO3↓+2NaCl |
①甲组实验1中产生气体的质量是
②依据甲乙两组的数据分别计算所配得的溶液中碳酸钠的质量分数;
甲:
测定结果与20%之间产生差异可能是实验原理、操作过程等因素引起的.