题目内容
如图所示是氨气分子示意图。试回答:
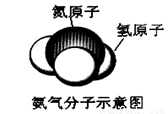
1)从微观角度分析:每个氨分子是由 构成;
2)从宏观角度分析:氨气是由 组成;
3)氨气与氯化氢气体发生化合反应生成氯化铵的化学方程式为 。
【答案】
一个氮原子和三个氢原子; 氢、氮二种元素; NH3+HCl=NH4Cl
【解析】
试题分析:(1)由图可知氨气分子由4个原子构成,其中3个氢原子,1个氮原子;
(2)由氨气的化学式NH3,可知 氨气是由氢、氮二种元素组成的;
(3)氨气与氯化氢气体发生化合反应生成氯化铵,反应物是氨气和氯化氢气体,生成物是氯化铵,得化学方程式为NH3+HCl=NH4Cl
考点:粒子的结构

练习册系列答案
相关题目
 11、氨气和氯化氢均是无色气体,某同学在实验中,观察到如图所示的实验现象后,得出以下结论,你认为其中不合理的是( )
11、氨气和氯化氢均是无色气体,某同学在实验中,观察到如图所示的实验现象后,得出以下结论,你认为其中不合理的是( ) 探究实验展示了化学的无穷魅力.我们在实验的过程中也提炼了许多探究方法.
探究实验展示了化学的无穷魅力.我们在实验的过程中也提炼了许多探究方法.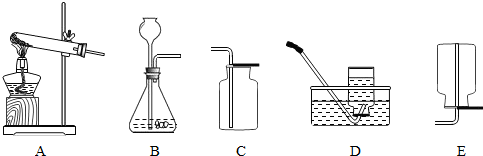
 、
、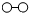 、
、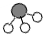 分别表示N2、H2、NH3.在催化剂表面(
分别表示N2、H2、NH3.在催化剂表面( 下图中表示催化剂表面)N2和H2反应合成氨的反应过程可用五张图表示如下:
下图中表示催化剂表面)N2和H2反应合成氨的反应过程可用五张图表示如下:
 微粒的基本性质”的实验探究,实验过程如下:
微粒的基本性质”的实验探究,实验过程如下: 表示氮原子,
表示氮原子, 表示氢原子)请结合图示回答问题:
表示氢原子)请结合图示回答问题: