题目内容
5.为测定氧化铜和铜混合物的组成情况,取16g混合物加入100g稀硫酸恰好反应后,加入100g氢氧化钠溶液恰好完全反应,过滤出17.8g沉淀,则混合物中铜元素与氧元素的质量最简比为( )| A. | 10:1 | B. | 9:1 | C. | 4:1 | D. | 1:1 |
分析 铜不与稀硫酸反应,氧化铜与稀硫酸反应生成硫酸铜和水,硫酸铜与氢氧化钠溶液反应生成氢氧化铜沉淀和硫酸钠,由生成氢氧化铜与氧化铜的质量,利用差量法,列出关系式计算出参加反应的氧化铜的质量,进而计算出混合物中铜元素与氧元素的质量比.
解答 解:氧化铜与稀硫酸反应生成硫酸铜和水,硫酸铜与氢氧化钠溶液反应生成氢氧化铜沉淀和硫酸钠,反应的化学方程式分别是H2SO4+CuO═CuSO4+H2O、2NaOH+CuSO4═Na2SO4+Cu(OH)2↓.
设参加反应的氧化铜的质量为x,
CuO~CuSO4~Cu(OH)2↓△m
80 98 98-80=18
x 17.8g-16g=1.8g
$\frac{80}{18}=\frac{x}{1.8g}$ x=8g
8g氧化铜中的氧元素含量为8g×$\frac{16}{64+16}$×100%=1.6g
则则混合物中铜元素与氧元素的质量最简比为(16g-1.6g):1.6g=9:1.
故选:B.
点评 本题难度不大,掌握根据化学方程式的计算并能灵活运用是正确解答本题的关键.

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
15.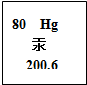 联合国环境规划署正式宣布:超过140个国家就全球第一部限制汞排放的国际公约《国际防治汞污染公约》达成一致.在元素周期表中汞元素的某些信息如图所示,下列有关汞的说法正确的是( )
联合国环境规划署正式宣布:超过140个国家就全球第一部限制汞排放的国际公约《国际防治汞污染公约》达成一致.在元素周期表中汞元素的某些信息如图所示,下列有关汞的说法正确的是( )
 联合国环境规划署正式宣布:超过140个国家就全球第一部限制汞排放的国际公约《国际防治汞污染公约》达成一致.在元素周期表中汞元素的某些信息如图所示,下列有关汞的说法正确的是( )
联合国环境规划署正式宣布:超过140个国家就全球第一部限制汞排放的国际公约《国际防治汞污染公约》达成一致.在元素周期表中汞元素的某些信息如图所示,下列有关汞的说法正确的是( )| A. | 汞在加热的条件下可以与氧气反应 | B. | 汞是一种非金属元素 | ||
| C. | 汞原子中含有80个中子 | D. | 汞的相对原子质量为200.6g |
12.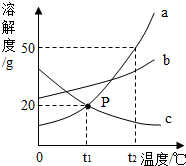 根据如图所示的溶解度曲线判断,下列说法正确的是( )
根据如图所示的溶解度曲线判断,下列说法正确的是( )
 根据如图所示的溶解度曲线判断,下列说法正确的是( )
根据如图所示的溶解度曲线判断,下列说法正确的是( )| A. | t1℃时,a、c饱和溶液中含有相等质量的溶质 | |
| B. | 将t2℃时a、b、c的饱和溶液降温到t1℃时都会析出晶体 | |
| C. | t1℃a、c两种物质的溶液中,溶质质量分数相等 | |
| D. | t2℃时a的饱和溶液溶质质量分数为33.3% |
10.分析推理是学习化学常用的一种思维方法,下列各选项分析推理正确的是( )
| A. | 二氧化硫是空气污染物,所以空气污染物都是由二氧化硫造成的 | |
| B. | 化合物是由不同种元素组成的纯净物,所以由不同种元素组成的纯净物一定是化合物 | |
| C. | 氧化物中一定含有氧元素,因此含有氧元素的物质一定是氧化物 | |
| D. | 单质是由同种元素组成,所以同种元素组成的物质一定是单质 |