题目内容
(2013?岐山县模拟)下面是某学习小组对Cu、Fe、Mg、Ag、Al五种金属相关知识的学习与探究.请你参与并回答问题:
(1)下列制品中,主要利用金属导电性的是

(2)铝的原子结构示意图为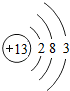 ,该原子在化学反应中易(填“得”或“失”)
,该原子在化学反应中易(填“得”或“失”)
(3)所给五种金属分别放入到同一盐酸中,最剧烈的反应的化学方程式为
(1)下列制品中,主要利用金属导电性的是
B
B
(填序号,下同).
(2)铝的原子结构示意图为
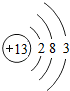 ,该原子在化学反应中易(填“得”或“失”)
,该原子在化学反应中易(填“得”或“失”)失
失
电子.(3)所给五种金属分别放入到同一盐酸中,最剧烈的反应的化学方程式为
Mg+2HCl═MgCl2+H2↑
Mg+2HCl═MgCl2+H2↑
.分析:(1)依据金属的用途和性质加以分析;(2)依据原子结构示意图中的最外层电子数进行判断;(3)根据方程式的书写方法考虑.
解答:解:(1)A.铁锅是主要利用铁的导热性;B.铜导线主要利用铜的导电性;C.铝箔主要利用铝的延展性.故答案为:B;
(2)从原子结构示意图上看,最外层电子数少于4个易失电子,最外层电子数等于或多于4个易得电子.故答案为:失;
(3)在金属活动性顺序表中,越排在前面的金属活动性最强.Cu、Fe、Mg、Ag、Al五种金属中Mg在金属活动性顺序表中最靠前.镁与稀盐酸反应,反应物是镁与氯化氢,产物是氯化镁与氢气,用观察法配平即可,所以方程式是:Mg+2HCl═MgCl2+H2↑.
故答案为:(1)B;(2)失;(3)Mg+2HCl═MgCl2+H2↑.
(2)从原子结构示意图上看,最外层电子数少于4个易失电子,最外层电子数等于或多于4个易得电子.故答案为:失;
(3)在金属活动性顺序表中,越排在前面的金属活动性最强.Cu、Fe、Mg、Ag、Al五种金属中Mg在金属活动性顺序表中最靠前.镁与稀盐酸反应,反应物是镁与氯化氢,产物是氯化镁与氢气,用观察法配平即可,所以方程式是:Mg+2HCl═MgCl2+H2↑.
故答案为:(1)B;(2)失;(3)Mg+2HCl═MgCl2+H2↑.
点评:此题考查各种金属的物理性质和在化学反应中原子得失电子的规律以及金属活动性顺序表.此题很简单,重在考查基础知识的运用.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目

 ,请据图回答下列问题:
,请据图回答下列问题: