题目内容
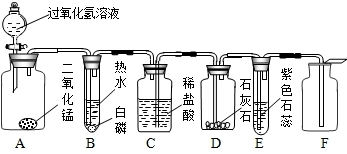
某同学模仿物理课上学到的“串联电路”,设计了如下气体制取与性质验证的组合实验.打开分液漏斗活塞后,A中出现大量气泡,B中白磷燃烧,C中液面下降.请看图回答问题:

(1)A中反应的化学方程式为:______.
(2)B中白磷能够燃烧的原因是______.
(3)D中的实验现象是______,反应的化学方程式为______.
(4)E中的实验现象是______,反应的化学方程式为______.
(5)用F装置收集气体的依据是______.
(6)现用大理石与稀盐酸反应制取二氧化碳气体,反应产生的二氧化碳气体的质量与加入的稀盐酸的质量关系如图所示.(提示:大理石中的杂质不发生反应,气体的溶解忽略不计)求:稀盐酸中溶质的质量分数是多少?
解:(1)过氧化氢在二氧化锰的作用下生成水和氧气,方程式为:2H2O2 2H2O+O2↑;
2H2O+O2↑;
(2)通入氧气后,白磷与氧气接触,温度达到白磷的着火点,使白磷具备了燃烧的三个条件,所以燃烧了;
(3)氧气不与盐酸反应,所以氧气把盐酸从C装置压人D装置,与石灰石反应,产生气泡,反应的方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(4)多余的二氧化碳进入E装置与水反应产生碳酸,使紫色的石蕊试液变成红色;反应的方程式为:CO2+H2O═H2CO3
(5)因为二氧化碳的密度比空气大,所以可以采用向上排空气法收集;
(6)根据坐标读出生成 2.2g二氧化碳,根据化学方程式的计算可以计算出氯化氢的质量,再计算出盐酸中溶质的质量分数.
解:设稀盐酸中溶质HCl的质量为X
CaCO3+2HCl═CaCl2+H2O+CO2↑
2×36.5 44
X 2.2g
 =
= X=3.65 g
X=3.65 g
稀盐酸中溶质HCl的质量分数为: ×100%=10%
×100%=10%
答:稀盐酸中溶质HCl的质量分数为10%.
故答案为:(1)2H2O2 2H2O+O2↑
2H2O+O2↑
(2)与氧气接触,温度达到着火点.
(3)C中液体进入D中,有气泡产生; CaCO3+2HCl═CaCl2+H2O+CO2↑
(4)导管口有气泡冒出,溶液由紫色变红色; CO2+H2O═H2CO3
(5)气体的密度比空气密度大
(6)解:设稀盐酸中溶质HCl的质量为X
CaCO3+2HCl═CaCl2+H2O+CO2↑
2×36.5 44
X 2.2g
 =
= X=3.65 g
X=3.65 g
稀盐酸中溶质HCl的质量分数为: ×100%=10%
×100%=10%
答:稀盐酸中溶质HCl的质量分数为10%.
分析:(1)过氧化氢在二氧化锰的作用下生成水和氧气;
(2)根据燃烧的条件分析:与氧气接触、温度达到着火点;
(3)盐酸在氧气的作用下被压进D中,与石灰石反应;
(4)根据二氧化碳与水反应生成碳酸能使石蕊试液变成红色分析;
(5)二氧化碳的密度比空气大,采用向上排空气法收集;
(6)读图,根据二氧化碳的质量计算氯化氢的质量,再根据溶质质量分数的公式计算.
点评:本题考查了气体的制取及有关的性质,属于基础性的考查,注意在根据化学方程式计算时要严格按照步骤计算.
 2H2O+O2↑;
2H2O+O2↑;(2)通入氧气后,白磷与氧气接触,温度达到白磷的着火点,使白磷具备了燃烧的三个条件,所以燃烧了;
(3)氧气不与盐酸反应,所以氧气把盐酸从C装置压人D装置,与石灰石反应,产生气泡,反应的方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(4)多余的二氧化碳进入E装置与水反应产生碳酸,使紫色的石蕊试液变成红色;反应的方程式为:CO2+H2O═H2CO3
(5)因为二氧化碳的密度比空气大,所以可以采用向上排空气法收集;
(6)根据坐标读出生成 2.2g二氧化碳,根据化学方程式的计算可以计算出氯化氢的质量,再计算出盐酸中溶质的质量分数.
解:设稀盐酸中溶质HCl的质量为X
CaCO3+2HCl═CaCl2+H2O+CO2↑
2×36.5 44
X 2.2g
 =
= X=3.65 g
X=3.65 g 稀盐酸中溶质HCl的质量分数为:
 ×100%=10%
×100%=10% 答:稀盐酸中溶质HCl的质量分数为10%.
故答案为:(1)2H2O2
 2H2O+O2↑
2H2O+O2↑(2)与氧气接触,温度达到着火点.
(3)C中液体进入D中,有气泡产生; CaCO3+2HCl═CaCl2+H2O+CO2↑
(4)导管口有气泡冒出,溶液由紫色变红色; CO2+H2O═H2CO3
(5)气体的密度比空气密度大
(6)解:设稀盐酸中溶质HCl的质量为X
CaCO3+2HCl═CaCl2+H2O+CO2↑
2×36.5 44
X 2.2g
 =
= X=3.65 g
X=3.65 g 稀盐酸中溶质HCl的质量分数为:
 ×100%=10%
×100%=10% 答:稀盐酸中溶质HCl的质量分数为10%.
分析:(1)过氧化氢在二氧化锰的作用下生成水和氧气;
(2)根据燃烧的条件分析:与氧气接触、温度达到着火点;
(3)盐酸在氧气的作用下被压进D中,与石灰石反应;
(4)根据二氧化碳与水反应生成碳酸能使石蕊试液变成红色分析;
(5)二氧化碳的密度比空气大,采用向上排空气法收集;
(6)读图,根据二氧化碳的质量计算氯化氢的质量,再根据溶质质量分数的公式计算.
点评:本题考查了气体的制取及有关的性质,属于基础性的考查,注意在根据化学方程式计算时要严格按照步骤计算.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目