题目内容
17.密闭容器中有X、Y、Z、W四种物质,在一定条件下完全发生反应后,测得数据如表,下列说法正确的是| 物 质 | X | Y | Z | W |
| 反应前质量/g | 10 | m | 8 | 7 |
| 反应后质量/g | 2 | 3 | 30 | 25 |
| A. | 若W为水,则X或Y必定为酸或碱 | |
| B. | 若Z为化合物,W为单质,则该反应一定为置换反应 | |
| C. | 若X、Y、Z、W均为化合物,则该反应一定为复分解反应 | |
| D. | 参加反应的X和Y的质量比为1:4 |
分析 反应后质量增加的属于生成物,反应后质量减少的属于反应物,反应后质量不变可能属于催化剂;本题可分析X、Z、W三种物质反应前后的质量变化情况,确定是反应物还是生成物;然后根据质量守恒定律确定Y是反应物还是生成物.
解答 解:由表中数据分析可知,反应前后,X的质量减少了10g-2g=8g,故X是反应物,参加反应的X的质量为8g;同理可以确定Z是生成物,生成的Z的质量为30g-8g=22g;W是生成物,生成的W的质量为25g-7g=18g;由质量守恒定律,Y应是反应物,且参加反应的Y的质量为22g+18g-8g=32g,故m的数值为32g+3g=35g.
A、若W为水,则X或Y不一定为酸或碱,甲烷与氧气反应也能生成水,故选项说法错误.
B、若Z为化合物,W为单质,则该反应不一定为置换反应,该反应的反应物可能均为化合物,不一定是置换反应,故选项说法错误.
C、若X、Y、Z、W均为化合物,则该反应不一定为复分解反应,如CO2+2NaOH═Na2CO3+H2O,故选项说法错误.
D、参加反应的X和Y的质量比为8g:32g=1:4,故选项说法正确.
故选:D.
点评 本题难度不大,考查的是质量守恒定律的应用,解题的关键是分析表中数据(反应后质量增加的属于生成物、质量减少的属于反应物),灵活运用质量守恒定律.

练习册系列答案
相关题目
18.下列应用与原理不一致的是( )
| A. | 活性炭除去水中色素和异味---吸附作用 | |
| B. | 洗洁精除去餐盘上的油污---乳化作用 | |
| C. | 油锅着火盖上锅盖---降低油的着火点 | |
| D. | 用Mg(OH)2治疗胃酸过多---中和反应 |
8.有关过氧化氢(H2O2)的叙述正确的是( )
| A. | 一个过氧化氢分子由一个氢分子和一个氧分子构成 | |
| B. | 保持过氧化氢化学性质的微粒是过氧化氢分子 | |
| C. | 过氧化氢由两个氢原子和两个氧原子构成 | |
| D. | 过氧化氢中氢氧元素的质量比是1:1 |
9.硅酸钠(Na2SiO3)是一种较好的防火材料,硅酸钠中硅元素的化合价为( )
| A. | +4 | B. | +2 | C. | +8 | D. | +2 |
6.生活中应用缓慢氧化的实例很多,下列反应中不属于缓慢氧化的是( )
| A. | 金属的锈蚀 | B. | 农家肥的腐熟 | C. | 植物的光合作用 | D. | 植物的呼吸作用 |
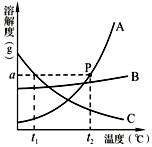 A、B、C三种物质的溶解度曲线如图所示.
A、B、C三种物质的溶解度曲线如图所示. 卢瑟福用a粒子(α粒子是带两个单位正电荷的氦原子核)轰击金箔的实验,推翻了汤姆生在1903年提出的原子结构模型,为建立现代原子理论打下了基础,但通过该实验的下述三种现象(如图),不能获得核外电子带有负电荷的结论.
卢瑟福用a粒子(α粒子是带两个单位正电荷的氦原子核)轰击金箔的实验,推翻了汤姆生在1903年提出的原子结构模型,为建立现代原子理论打下了基础,但通过该实验的下述三种现象(如图),不能获得核外电子带有负电荷的结论.