题目内容
某工厂排出的废液中可能含有盐酸、碳酸钠、氯化铜、氯化钠中的一种或几种.现向该混合溶液中滴入氢氧化钡溶液,开始时无明显现象,片刻后有沉淀生成.则该废液中一定含有 ;一定不含有 .
【答案】分析:依据废液中物质的可能含有情况分析,盐酸、碳酸钠、氯化铜、氯化钠四物质间碳酸钠和盐酸能够生成二氧化碳,所以两者不可能共存,滴加氢氧化钡后开始没有现象,说明废液中含有盐酸,从而说明废液中不含碳酸钠,片刻后有沉淀生成则废液中含有氯化铜,原因是盐酸耗尽后氯化铜和氢氧化钡能够生成氢氧化铜的蓝色沉淀,但氯化钠是否含有无法确定;
解答:解:由于盐酸、碳酸钠、氯化铜、氯化钠四物质中碳酸钠和盐酸能够生成二氧化碳,所以两者不可能共存,滴加氢氧化钡后开始没有现象,说明废液中含有盐酸,从而说明废液中不含碳酸钠,片刻后有沉淀生成则废液中含有氯化铜,原因是盐酸耗尽后氯化铜和氢氧化钡能够生成氢氧化铜的蓝色沉淀,但氯化钠是否含有无法确定;
故答案为:盐酸、氯化铜;碳酸钠;
点评:熟悉常见物质和离子的检验,熟悉常见物质的特征性颜色以及特征性反应,只有这样才能很好的完成物质推断题.
解答:解:由于盐酸、碳酸钠、氯化铜、氯化钠四物质中碳酸钠和盐酸能够生成二氧化碳,所以两者不可能共存,滴加氢氧化钡后开始没有现象,说明废液中含有盐酸,从而说明废液中不含碳酸钠,片刻后有沉淀生成则废液中含有氯化铜,原因是盐酸耗尽后氯化铜和氢氧化钡能够生成氢氧化铜的蓝色沉淀,但氯化钠是否含有无法确定;
故答案为:盐酸、氯化铜;碳酸钠;
点评:熟悉常见物质和离子的检验,熟悉常见物质的特征性颜色以及特征性反应,只有这样才能很好的完成物质推断题.

练习册系列答案
 快捷英语周周练系列答案
快捷英语周周练系列答案
相关题目
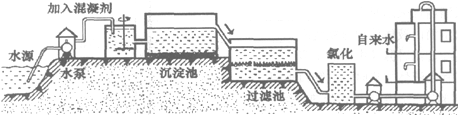
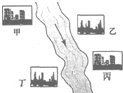 HCl中的一种.某环保小组对河水监测时发现:甲处河水呈无色;乙处河水呈红褐色;丙处河水由浑变清;丁处产生气泡,河水澄清.请回答:
HCl中的一种.某环保小组对河水监测时发现:甲处河水呈无色;乙处河水呈红褐色;丙处河水由浑变清;丁处产生气泡,河水澄清.请回答: