题目内容
对下列实验的评价,正确的是( )
| A、某无色溶液滴入酚酞试液显红色,该溶液一定显碱性 |
| B、某溶液滴加氯化钡,再滴加稀硝酸,产生白色沉淀,该溶液中一定含硫酸根 |
| C、某溶液滴加硝酸银,再滴加稀硝酸,产生白色沉淀,该溶液一定是盐酸 |
| D、某固体加入稀盐酸,产生无色气体,该固体中一定含有碳酸根 |
考点:化学实验方案设计与评价,酸碱指示剂及其性质,常见离子的检验方法及现象
专题:简单实验方案的设计与评价
分析:A、根据酚酞试液遇到碱性溶液变红进行解答;
B、根据某溶液滴加氯化钡,再滴加稀硝酸,产生白色沉淀,该溶液中不一定含硫酸根进行解答;
C、根据只要含有氯离子的溶液中硝酸银,再滴加稀硝酸,就会产生白色沉淀进行解答;
D、根据金属和盐酸反应也会放出气体进行解答.
B、根据某溶液滴加氯化钡,再滴加稀硝酸,产生白色沉淀,该溶液中不一定含硫酸根进行解答;
C、根据只要含有氯离子的溶液中硝酸银,再滴加稀硝酸,就会产生白色沉淀进行解答;
D、根据金属和盐酸反应也会放出气体进行解答.
解答:解:A、酚酞试液遇到碱性溶液变红,所以某无色溶液滴入酚酞试液显红色,该溶液一定显碱性,故A正确;
B、某溶液滴加氯化钡,再滴加稀硝酸,产生白色沉淀,该溶液中不一定含硫酸根,也有可能含有银离子,生成氯化银白色沉淀,故B错误;
C、只要含有氯离子的溶液中硝酸银,再滴加稀硝酸,就会产生白色沉淀,所以溶液不一定是盐酸,故C错误;
D、金属和盐酸反应也会放出气体,所以某固体加入稀盐酸,产生无色气体,该固体中不一定含有碳酸根,故D错误.
故选:A.
B、某溶液滴加氯化钡,再滴加稀硝酸,产生白色沉淀,该溶液中不一定含硫酸根,也有可能含有银离子,生成氯化银白色沉淀,故B错误;
C、只要含有氯离子的溶液中硝酸银,再滴加稀硝酸,就会产生白色沉淀,所以溶液不一定是盐酸,故C错误;
D、金属和盐酸反应也会放出气体,所以某固体加入稀盐酸,产生无色气体,该固体中不一定含有碳酸根,故D错误.
故选:A.
点评:解答本题要根据物质的性质选择合适的物质进行实验,要求同学们加强对物质性质的记忆,以便灵活应用.

练习册系列答案
相关题目
按下列实验装置进行相关实验,其中不能达到实验目的是.
A、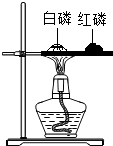 比较红磷、白磷着火点 |
B、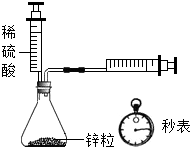 定量测定化学反应速率 |
C、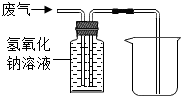 除去废气中的CO2,并收集CO |
D、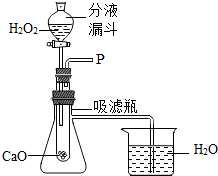 验证CaO和水反应的热效应 |
下列有关实验设计达不到实验目的是( )
A、 将固体药品装入试管中 |
B、 探究空气中氧气体积分数 |
C、 验证CO2 密度比空气大且不能燃烧也不支持燃烧 |
D、 收集H2 |
2013年12月14日,中国发射的“嫦娥三号”火箭携带“玉兔号”月球车成功登陆月球.在此过程中属于化学变化的是( )
| A、火箭点火发射 |
| B、火箭进入轨道 |
| C、火箭落月成功 |
| D、嫦娥三号与玉兔号分离 |
下列实验现象描述不正确的是( )
| A、红磷燃烧产生大量的白烟 |
| B、硫在空气中燃烧,产生淡蓝色火焰 |
| C、硫酸铜溶液中滴入氢氧化钠溶液,有蓝色沉淀生成 |
| D、氯化铵固体和熟石灰混合研磨,生成无色无味的气体 |
如图示的基本实验操作中,正确的是( )
A、 取用粉末固体 |
B、 加热液体 |
C、 检查气密性 |
D、 点燃酒精灯 |
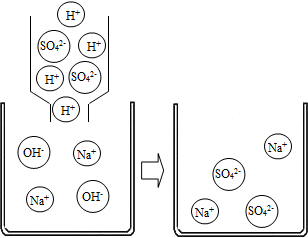 某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格).
某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格).


