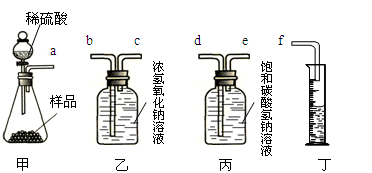
��Ŀ����
ij�����������Ĵ����к�������NaCl���ʣ����Ʒ��װ���ϱ��У�̼���ơ�96%��Ϊ��֤ʵ�ò�Ʒ��̼���Ƶĺ�����ijͬѧȡ12g����Ʒ�����ձ��У��Ƶ��ձ�����Ʒ������Ϊ132.0g�ٰ�100gϡ����ƽ���ֳ�4�μ����ձ��У�ÿ�γ�ַ�Ӧ���ձ���ʣ�������������£���ÿ�η�Ӧ������CO2���嶼ȫ�����ձ����ݳ���
|
����ϡ������� |
1 |
2 |
3 |
4 |
|
����ϡ��������/g |
25 |
25 |
25 |
25 |
|
��ַ�Ӧ���ձ���ʣ����������/g |
155.2 |
178.4 |
202.6 |
227.6 |
������ݱ������ݷ������ٵ�1�γ�ַ�Ӧ�������CO2������������ ��g
�ڸò�Ʒ��̼���Ƶ����������Ƕ��٣��ò�Ʒ�Ƿ�ϸ������ش𣬼�������ȷ��0.1%��
��1.8g�� ��88.3%�����ϸ�
��������
����������ٸ��ݱ������ݿɵã���һ�μ���ϡ�����ַ�Ӧ�������������̼������Ϊ132g+25��155.2g=1.8g��
����Ʒ��ȫ��Ӧʱ������CO2������Ϊ=132g+100g��227.6g=4.4g
������4.4gCO2����̼���Ƶ�����Ϊx
Na2CO3+2HCl�T2NaCl+H2O+CO2��
106 44
x 4.4g

x=10.6g
�ò�Ʒ��̼���Ƶ���������= ��100%=88.3%
��100%=88.3%
��96%��88.3%
��ò�Ʒ��Na2CO3�������������ϸ�
�𣺢ٵ�һ�μ���ϡ�����ַ�Ӧ�����ɶ�����̼������1.8g���ڸò�Ʒ��̼���Ƶ�����������88.3%���ò�Ʒ��̼���Ƶ������������ϸ�
���㣺���ݻ�ѧ��Ӧ����ʽ�ļ��㣮
����������ÿ�μ���ϡ�����ַ�Ӧǰ�����ʵ��������ɵõ���ַ�Ӧ������������̼���������ɴ������Է�Ӧ������������жϣ���Ϊ�����Ļ���˼·��

| ����ϡ������� | 1 | 2 | 3 | 4 |
| ����ϡ��������/g | 25 | 25 | 25 | 25 |
| ��ַ�Ӧ���ձ���ʣ����������/g | 155.2 | 178.4 | 202.6 | 227.6 |
�ڸò�Ʒ��̼���Ƶ����������Ƕ��٣��ò�Ʒ�Ƿ�ϸ������ش𣬼�������ȷ��0.1%��