题目内容
如图为“хх”钙片商品标签图,请根据标签的有关信息完成下列各题.小花同学为测定其中碳酸钙的含量标注是否属实,她取出10片钙片,研碎后放入小烧杯中,再加入50g稀盐酸,在T至T3时间段,测得反应剩余物的质量变化如下:
(1)生成的二氧化碳的质量是______;
(2)通过计算______判断该钙片中碳酸钙的含量标注是否属实.
| 时 间 | T | T1 | T2 | T3 |
| 反应剩余物质量(g) | 70 | 65 | 63、4 | 63.4 |

【答案】分析:(1)根据质量守恒定律:反应前后物质的质量不变,进行解答;
(2)根据化学式方程式,依据生成二氧化碳的质量进行分析解答本题.
解答:解:(1)根据质量守恒定律,生成的二氧化碳的质量为:70-63.4=6.6g;
故答案为:6.6g;
(2)解:设10片样品中碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
X 6.6g
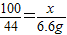 ,解答 x=15g;
,解答 x=15g;
每片含碳酸钙的质量为: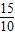 =1.5g,与标签中钙含量相符;
=1.5g,与标签中钙含量相符;
故钙片中碳酸钙的含量标注属实.
点评:本题考查学生根据化学方程式和质量守恒定律进行分析解题的能力.
(2)根据化学式方程式,依据生成二氧化碳的质量进行分析解答本题.
解答:解:(1)根据质量守恒定律,生成的二氧化碳的质量为:70-63.4=6.6g;
故答案为:6.6g;
(2)解:设10片样品中碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
X 6.6g
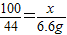 ,解答 x=15g;
,解答 x=15g; 每片含碳酸钙的质量为:
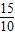 =1.5g,与标签中钙含量相符;
=1.5g,与标签中钙含量相符;故钙片中碳酸钙的含量标注属实.
点评:本题考查学生根据化学方程式和质量守恒定律进行分析解题的能力.

练习册系列答案
相关题目
 如图为“хх”钙片商品标签图,请根据标签的有关信息完成下列各题.
如图为“хх”钙片商品标签图,请根据标签的有关信息完成下列各题. 如图为“хх”钙片商品标签图,请根据标签的有关信息完成下列各题.主要成分碳酸钙的化学式是CaCO3
如图为“хх”钙片商品标签图,请根据标签的有关信息完成下列各题.主要成分碳酸钙的化学式是CaCO3 化学就在我们身边,它与我们的生活息息相关.
化学就在我们身边,它与我们的生活息息相关. 如图为“хх”钙片商品标签图,请根据标签的有关信息:下列说法正确的是( )
如图为“хх”钙片商品标签图,请根据标签的有关信息:下列说法正确的是( ) 如图为“хх”钙片商品标签图,请根据标签的有关信息完成下列各题.
如图为“хх”钙片商品标签图,请根据标签的有关信息完成下列各题.