题目内容
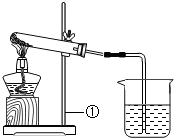 有一包白色的固体粉末,可能是NaHCO3、NaOH中的一种或二种,化学小组对其组成进行如图所示的实验:
有一包白色的固体粉末,可能是NaHCO3、NaOH中的一种或二种,化学小组对其组成进行如图所示的实验:资料:1.酒精灯加热温度约500~600℃.
2.NaOH 318.4℃熔化不分解,1390℃沸腾不分解.
3.Na2CO3+CaCl2→CaCO3↓+2NaCl.
4.Na2CO3溶液呈碱性;CaCl2溶液呈中性
(1)完成实验报告的内容:
| 实验操作 | 实验现象 | 实验结论 |
| ①取一定量的白色粉末加热,将产生的气体通入小烧杯中,至无气体产生时,停止加热 (小烧杯内盛有澄清的石灰水) |
试管内壁有无色液滴,石灰水变浑浊,试管内剩余白色固体物质 | 粉末中一定含有 反应的化学方程式是 |
| ②取实验①所剩余白色固体少量于试管中,向试管中加入稀盐酸 | 实验①所剩余白色固体中一定含有 反应的化学方程式是 |
分析:(1)根据试管中的现象和题中所给的资料进行分析;
(2)根据氢氧化钠溶液显碱性,将碳酸根离子屏蔽后检验酸碱性就可以鉴别.
(2)根据氢氧化钠溶液显碱性,将碳酸根离子屏蔽后检验酸碱性就可以鉴别.
解答:解:碳酸氢钠受热后会分解成碳酸钠、水和二氧化碳,氢氧化钠在受热后不会分解,加热后,试管内壁有无色液滴,产生无色气体,石灰水变浑浊,所以一定存在碳酸氢钠,
氢氧化钠和盐酸反应不会生成气体,碳酸钠和盐酸反应会生成氯化钠、水和二氧化碳,
(2)检验氢氧化钠需要将其他的显碱性的物质屏蔽后才能用酚酞检验,
故答案为:加水溶解,加入过量的CaCl2溶液使沉淀完全,静置后向上层清液中滴加酚酞溶液.若溶液变红,则产物中有NaOH;若溶液不变色,则产物中没有NaOH
氢氧化钠和盐酸反应不会生成气体,碳酸钠和盐酸反应会生成氯化钠、水和二氧化碳,
| 实验操作 | 实验现象 | 实验结论 | ||||
| ①取一定量的白色粉末加热,将产生的气体通入小烧杯中,至无气体产生时,停止加热 (小烧杯内盛有澄清的石灰水) |
试管内壁有无色液滴,石灰水变浑浊,试管内剩余白色固体物质 | 粉末中一定含有 NaHCO3反应的化学方程式是2NaHCO3
| ||||
| ②取实验①所剩余白色固体少量于试管中,向试管中加入稀盐酸 | 有气体产生 | 实验①所剩余白色固体中一定含有 Na2CO3;反应的化学方程式Na2CO3+2HCl=2NaCl+H2O+CO2↑ |
故答案为:加水溶解,加入过量的CaCl2溶液使沉淀完全,静置后向上层清液中滴加酚酞溶液.若溶液变红,则产物中有NaOH;若溶液不变色,则产物中没有NaOH
点评:在解此类题时,首先分析题中考查的问题,然后结合学过的知识和题中所给的知识进行分析解答.

练习册系列答案
相关题目
(7分)有一包白色的固体粉末,可能是NaHCO3、NaOH中的一种或二种,化学小组对其组成进行如图所示的实验:
资料:1.酒精灯加热温度约500~600 ℃;
2. NaOH 318.4℃熔化不分解,1390 ℃沸腾不分解;
3. Na2CO3+CaCl2→CaCO3↓+ 2NaCl
4. Na2CO3溶液呈碱性;CaCl2溶液呈中性
(1)完成实验报告的内容:
| 实验操作 | 实验现象 | 实验结论 |
| ①取一定量的白色粉末加热,将产生的气体通入小烧杯中,至无气体产生时,停止加热 (小烧杯内盛有澄清的石灰水) | 试管内壁有无色液滴,石灰水变浑浊,试管内剩余白色固体物质 | 粉末中一定含有 反应的化学方程式是 |
| ②取实验①所剩余白色固体少量于试管中,向试管中加入稀盐酸 | | 实验①所剩余白色固体中一定含有 ; 反应的化学方程式是 |
(7分)有一包白色的固体粉末,可能是NaHCO3、NaOH中的一种或二种,化学小组对其组成进行如图所示的实验:
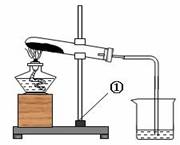
资料:1.酒精灯加热温度约500~600 ℃;
2. NaOH 318.4℃熔化不分解,1390 ℃沸腾不分解;
3. Na2CO3+CaCl2→CaCO3↓+ 2NaCl
4. Na2CO3溶液呈碱性;CaCl2溶液呈中性
(1)完成实验报告的内容:
|
实验操作 |
实验现象 |
实验结论 |
|
①取一定量的白色粉末加热,将产生的气体通入小烧杯中,至无气体产生时,停止加热 (小烧杯内盛有澄清的石灰水) |
试管内壁有无色液滴,石灰水变浑浊,试管内剩余白色固体物质
|
粉末中一定含有
反应的化学方程式是
|
|
②取实验①所剩余白色固体少量于试管中,向试管中加入稀盐酸
|
|
实验①所剩余白色固体中一定含有 ; 反应的化学方程式是
|
(2)为确定白色粉末中是否含有NaOH的方案是:取实验①所剩余白色固体少量, 。
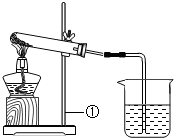 有一包白色的固体粉末,可能是NaHCO3、NaOH中的一种或二种,化学小组对其组成进行如图所示的实验:
有一包白色的固体粉末,可能是NaHCO3、NaOH中的一种或二种,化学小组对其组成进行如图所示的实验:
资料:1.酒精灯加热温度约500~600℃.
2.NaOH 318.4℃熔化不分解,1390℃沸腾不分解.
3.Na2CO3+CaCl2→CaCO3↓+2NaCl.
4.Na2CO3溶液呈碱性;CaCl2溶液呈中性
(1)完成实验报告的内容:
| 实验操作 | 实验现象 | 实验结论 |
| ①取一定量的白色粉末加热,将产生的气体通入小烧杯中,至无气体产生时,停止加热 (小烧杯内盛有澄清的石灰水) | 试管内壁有无色液滴,石灰水变浑浊,试管内剩余白色固体物质 | 粉末中一定含有 ______ 反应的化学方程式是 ______ |
| ②取实验①所剩余白色固体少量于试管中,向试管中加入稀盐酸 | ______ | 实验①所剩余白色固体中一定含有 ______; 反应的化学方程式是 ______ |
(2011?怀柔区二模)有一包白色的固体粉末,可能是NaHCO3、NaOH中的一种或二种,化学小组对其组成进行如图所示的实验:
资料:1.酒精灯加热温度约500~600℃.
2.NaOH 318.4℃熔化不分解,1390℃沸腾不分解.
3.Na2CO3+CaCl2→CaCO3↓+2NaCl.
4.Na2CO3溶液呈碱性;CaCl2溶液呈中性
(1)完成实验报告的内容:
Na2CO3+H2O+CO2↑
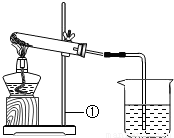
资料:1.酒精灯加热温度约500~600℃.
2.NaOH 318.4℃熔化不分解,1390℃沸腾不分解.
3.Na2CO3+CaCl2→CaCO3↓+2NaCl.
4.Na2CO3溶液呈碱性;CaCl2溶液呈中性
(1)完成实验报告的内容:
| 实验操作 | 实验现象 | 实验结论 |
| ①取一定量的白色粉末加热,将产生的气体通入小烧杯中,至无气体产生时,停止加热 (小烧杯内盛有澄清的石灰水) | 试管内壁有无色液滴,石灰水变浑浊,试管内剩余白色固体物质 | 粉末中一定含有 ______ 反应的化学方程式是 ______ |
