题目内容
14.小明在实验室里加热31.6g高锰酸钾制取氧气,完全反应后剩余固体质量为28.4g,将剩余固体溶解、过滤、烘干上,回收二氧化锰.(2KMnO4 $\frac{\underline{\;\;△\;\;}}{\;}$ K2MnO4+MnO2+O2↑)请计算:
(1)生成氧气的质量为3.2 g.
(2)回收二氧化锰的质量.
分析 (1)根据质量守恒定律,求出生成氧气的质量;
(2)根据生成氧气的质量,利用反应的化学方程式,得出各物质之间的质量比,列出比例式,即可计算出回收二氧化锰的质量.
解答 解:(1)根据质量守恒定律,当固体质量变为28.4g时,生成氧气的质量为31.6g-28.4g=3.2g;故填:3.2;
(2)设生成MnO2的质量为x
2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
87 32
x 3.2g
$\frac{87}{x}=\frac{32}{3.2g}$
x=8.7g
答:回收二氧化锰的质量为8.7g.
点评 本题主要考查学生对化学反应方程式的书写,以及运用方程式进行计算的能力.

练习册系列答案
相关题目
4.下列所给的是实验室制取某些气体的仪器(如图所示)和试剂.请认真审题,完成下列问题.
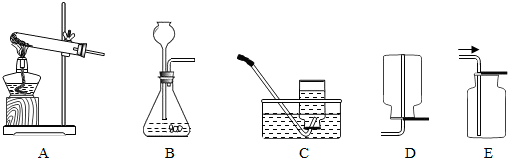
试剂:过氧化氢、二氧化锰、大理石、稀盐酸
(1)在图中的气体发生装置中,有一处错误,请改正错误长颈漏斗下端应伸入液面以下.
(2)完成下列表格:
(3)检验氧气的方法是将带火星的木条伸入集气瓶内,若木条复燃,则证明是氧气.
(4)验满二氧化碳的方法是将气体通入澄清的石灰水,若澄清的石灰水变浑浊,则证明是二氧化碳.

试剂:过氧化氢、二氧化锰、大理石、稀盐酸
(1)在图中的气体发生装置中,有一处错误,请改正错误长颈漏斗下端应伸入液面以下.
(2)完成下列表格:
| 制取气体 | 发生装置(填序号) | 收集装置(填序号) |
| 氧气 | ||
| 二氧化碳 |
(4)验满二氧化碳的方法是将气体通入澄清的石灰水,若澄清的石灰水变浑浊,则证明是二氧化碳.
5.分析推理是化学常用的一种学习方法,下列推理正确的是( )
| A. | MnO2可以加快H2O2分解产生O2的速率,所以催化剂一定加快化学反应速率 | |
| B. | 钙原子核钙离子的质子数都是2O,所以质子数相同的微粒一定是同种元素 | |
| C. | 化学变化中分子一定发生改变,所以分子发生改变的变化一定是化学变化 | |
| D. | Na+、Mg2+、Cl-的最外层电子数均为8,由此得出离子的最外层电子数均为8 |
2.下列化学变化中吸收热量的是( )
| A. | 氢气还原氧化铜 | B. | 铁在氧气中燃烧 | C. | 锌和稀硫酸反应 | D. | 动植物的呼吸 |
