题目内容
向盛有12.6g碳酸氢钠固体的烧杯中,加入100.5g硫酸溶液恰好反应.反应的化学方程式为:2NaHCO3+H2SO4═Na2SO4+2H2O+2CO2↑
回答下列问题:
(1)当碳酸氢钠与硫酸溶液完全反应时,所产生二氧化碳的质量为多少.
(2)硫酸溶液中溶质质量分数为多少?
(3)反应后,所得硫酸钠溶液的溶质质量分数为多少?
回答下列问题:
(1)当碳酸氢钠与硫酸溶液完全反应时,所产生二氧化碳的质量为多少.
(2)硫酸溶液中溶质质量分数为多少?
(3)反应后,所得硫酸钠溶液的溶质质量分数为多少?
分析:已知碳酸氢钠固体的质量,根据反应的化学方程式可以计算反应的硫酸质量,生成的硫酸钠质量,产生的二氧化碳质量,进一步可以计算硫酸溶液、硫酸钠溶液的质量分数.
解答:解:设反应的硫酸、生成的硫酸钠、二氧化碳的质量分别为x、y、z,
2NaHCO3+H2SO4═Na2SO4+2H2O+2CO2↑,
168 98 142 88
12.6g x y z
=
,
=
,
=
,
x=7.35g,y=10.65g,z=6.6g,
(1)生成二氧化碳的质量为6.6g.
(2)硫酸溶液中溶质质量分数为:
×100%=7.3%,
答:硫酸溶液中溶质质量分数为7.3%.
(3)所得硫酸钠溶液的质量为:12.6g+100.5g-6.6g=106.5g,
反应后,所得硫酸钠溶液的溶质质量分数为:
×100%=10%,
答:所得硫酸钠溶液的溶质质量分数为10%.
2NaHCO3+H2SO4═Na2SO4+2H2O+2CO2↑,
168 98 142 88
12.6g x y z
| 168 |
| 98 |
| 12.6g |
| x |
| 168 |
| 142 |
| 12.6g |
| y |
| 168 |
| 88 |
| 12.6g |
| z |
x=7.35g,y=10.65g,z=6.6g,
(1)生成二氧化碳的质量为6.6g.
(2)硫酸溶液中溶质质量分数为:
| 7.35g |
| 100.5g |
答:硫酸溶液中溶质质量分数为7.3%.
(3)所得硫酸钠溶液的质量为:12.6g+100.5g-6.6g=106.5g,
反应后,所得硫酸钠溶液的溶质质量分数为:
| 10.65g |
| 106.5g |
答:所得硫酸钠溶液的溶质质量分数为10%.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,只要注意解答的规范性、计算的准确性即可.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
中考前复习,小芳打算把厨房中盛有淀粉、NaCl、Na2CO3、NaHCO3的调料盒贴上标签.中考结束帮妈妈做家务.请你帮助小芳完成如下探究过程:
实验准备工作:将四种调料盒编号为A、B、C、D
(1)取四种白色固体各少量于试管中,加适量水充分振荡.通过实验将B盒贴上写有 的标签
(2)取A、C、D各少量于试管中,实验记录如下,填齐下表:
编号A的调料盒为
(3)查阅资料:
资料1:碳酸钠和碳酸氢钠在一定条件下可以相互转化,转化过程如图所示:
NaHCO3
Na2CO3
资料2:
(4)依据资料,帮助小芳完成如下实验方案设计来区别NaHCO3和Na2CO3:
实验方案1:小芳拟定用如图所示装置进行实验,若洁净试管中的物质为碳酸氢钠,小芳观察到的现象有 .
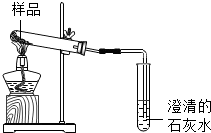
实验方案2:取两种待检测样品制成20°C的饱和溶液,取两种饱和溶液适量分别于试管中,向试管中通入二氧化碳, (写出实验现象和对应结论).
实验方案3:设计下列实验请填现象和结论
实验准备工作:将四种调料盒编号为A、B、C、D
(1)取四种白色固体各少量于试管中,加适量水充分振荡.通过实验将B盒贴上写有
(2)取A、C、D各少量于试管中,实验记录如下,填齐下表:
| 样品 实验现象 所加试剂 |
A | C | D |
| 无现象 | 有气泡 |
(3)查阅资料:
资料1:碳酸钠和碳酸氢钠在一定条件下可以相互转化,转化过程如图所示:
NaHCO3
| △ |
| H2O、CO2 |
资料2:
| 温度 溶解度 盐 |
10℃ | 20℃ | 30℃ | 40℃ |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
实验方案1:小芳拟定用如图所示装置进行实验,若洁净试管中的物质为碳酸氢钠,小芳观察到的现象有

实验方案2:取两种待检测样品制成20°C的饱和溶液,取两种饱和溶液适量分别于试管中,向试管中通入二氧化碳,
实验方案3:设计下列实验请填现象和结论
| 实验操作 | 实验现象 | 结论 |
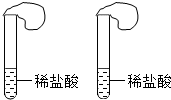 两个试管各加足量且相等的稀盐酸, 试管上系的气球里各装入106克 两种白色粉末,同时倒入盐酸中. |
 向盛有12.60g碳酸氢钠固体的烧杯中加入100.5g硫酸溶液恰好完全反应.反应过程用精密仪器测得烧杯连同药品的质量(m)与反应时间(t)的关系如下图所示.烧杯连同药品的起始质量为200.0g.反应的化学方程式为2NaHCO3+H2SO4═Na2SO4+2H2O+2CO2↑
向盛有12.60g碳酸氢钠固体的烧杯中加入100.5g硫酸溶液恰好完全反应.反应过程用精密仪器测得烧杯连同药品的质量(m)与反应时间(t)的关系如下图所示.烧杯连同药品的起始质量为200.0g.反应的化学方程式为2NaHCO3+H2SO4═Na2SO4+2H2O+2CO2↑
