题目内容
20.在CuCl2和FeCl2的混合物溶液中加入一定量的锌,充分反应后,过滤,向滤渣中加入稀盐酸,有气体生成,则滤渣中一定含有( )| A. | Cu、Zn、Fe | B. | Cu、Fe | C. | Cu、Zn | D. | Zn、Fe |
分析 在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢,位于前面的金属能把排在它后面的金属从其盐溶液中置换出来,进行分析判断.
解答 解:根据在金属活动性顺序中,锌>铁>氢>铜,锌的金属活动性比铁、铜强,在CuCl2和FeCl2的混合物溶液中加入一定量的锌,锌先与氯化铜溶液反应生成氯化锌溶液和铜,氯化铜反应完,若还有锌,锌才能与氯化亚铁溶液反应生成氯化锌溶液和铁;由题意,充分反应后,过滤,向滤渣中加入稀盐酸,有气体生成,铜不与稀盐酸反应,说明滤渣中存在能与稀盐酸反应的金属,一定含有铁,可能含有锌;故滤渣中一定含有Cu、Fe.
故选:B.
点评 本题难度不是很大,熟练掌握金属的化学性质、综合考虑各种出现的情况是正确解答此类题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.推理是学习化学的一种重要方法.下列的推理正确的是( )
| A. | 酸与碱反应生成盐和水,所以生成盐和水的反应一定是酸与碱的反应 | |
| B. | 向某溶液中滴加无色酚酞试液,酚酞试液不变色,说明该溶液一定显酸性 | |
| C. | 酸和碱的溶液能与指示剂反应,所以所有的酸和碱都能使指示剂变色 | |
| D. | 向某溶液中滴加紫色石蕊试液,紫色石蕊试液变红色,说明该溶液一定显酸性 |
9.森林发生火灾时,可以用爆炸灭火的方法,将灭火弹抛到火场爆炸将火扑灭.关于爆炸灭火的原因分析不合理的是( )
| A. | 爆炸气浪使燃烧暂时处于缺氧的状态 | |
| B. | 爆炸气浪降低了可燃物的温度 | |
| C. | 爆炸气浪降低了可燃物的着火点 | |
| D. | 爆炸气浪冲起的沙土覆盖了可燃物,隔绝了空气 |
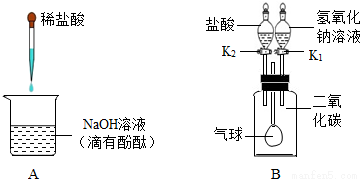
 实验中,小红将氢氧化钠(NaOH)溶液滴加到金属铝中,发现有气泡产生,为了解该气体的成分,实验小组进行了以下探究:
实验中,小红将氢氧化钠(NaOH)溶液滴加到金属铝中,发现有气泡产生,为了解该气体的成分,实验小组进行了以下探究: