题目内容
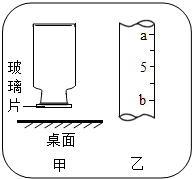
 (2013?南昌)如图是甲、乙两种固体的溶解度曲线.下列说法中正确的是( )
(2013?南昌)如图是甲、乙两种固体的溶解度曲线.下列说法中正确的是( )分析:A、比较物质的溶解度大小须确定温度;
B、据t1℃时甲的溶解度分析解答;
C、据乙的溶解度随温度的降低的变化情况分析判断;
D、据甲的溶解度随温度的升高溶解度变化及溶质的质量分数计算方法分析解答.
B、据t1℃时甲的溶解度分析解答;
C、据乙的溶解度随温度的降低的变化情况分析判断;
D、据甲的溶解度随温度的升高溶解度变化及溶质的质量分数计算方法分析解答.
解答:解:A、不知温度,无法比较甲、乙溶解度大小,故错误;
B、t1℃时甲的溶解度是30g,所以该温度下50g水中最多溶解15g甲,正确;
C、乙的溶解度随温度的降低而减小,所以t2℃时乙的饱和溶液降温至t1℃依然是饱和溶液,故错误;
D、甲的溶解度随温度的升高而增大,溶质质量分数=
×100%,所以将t1℃时甲的饱和溶液升温至t2℃,溶质、溶剂的质量不变,溶质的质量分数不变,故错误;
故选B.
B、t1℃时甲的溶解度是30g,所以该温度下50g水中最多溶解15g甲,正确;
C、乙的溶解度随温度的降低而减小,所以t2℃时乙的饱和溶液降温至t1℃依然是饱和溶液,故错误;
D、甲的溶解度随温度的升高而增大,溶质质量分数=
| 溶质的质量 |
| 溶液的质量 |
故选B.
点评:本题考查了溶解度曲线意义的应用,能较好考查学生应用知识分析、解决问题的能力.

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目
 ”与“
”与“ 分别表示不同元素的原子.图中X处的粒子示意图是( )
分别表示不同元素的原子.图中X处的粒子示意图是( )
 (2013?南昌)+物质王国举行一场趣味篮球赛.某对由铁、二氧化碳、稀硫酸、氢氧化钙、氯化铜五名“队员”组成,比赛中,由氯化铜“队员”发球,“队员”间传接球,最后由D位置“队员”投篮进球完成有效进攻.传接球“队员”间物质必须能相互反应,场上“队员”位置及传球路线如图.(1)已知D位置上投篮的“队员”是个灭火“能手”,则D位置“队员”代表的物质是
(2013?南昌)+物质王国举行一场趣味篮球赛.某对由铁、二氧化碳、稀硫酸、氢氧化钙、氯化铜五名“队员”组成,比赛中,由氯化铜“队员”发球,“队员”间传接球,最后由D位置“队员”投篮进球完成有效进攻.传接球“队员”间物质必须能相互反应,场上“队员”位置及传球路线如图.(1)已知D位置上投篮的“队员”是个灭火“能手”,则D位置“队员”代表的物质是