题目内容
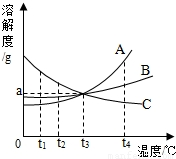
如图是A、B、C三种固体物质(固体组成与溶质相同)的溶解度曲线.在t1℃时,将质量为a g的A、B、C三种物质分别加入100g水中,根据图示回答下列问题:(1)三种物质中,随温度升高溶解度减小的物质是 ;
(2)t1℃时,所得三种物质的溶液中为不饱溶液的是 ;
(3)若使这三种溶液溶质的质量分数相等,则温度应由t1℃升至 ℃;
(4)若将温度由t1℃升至 t4℃时,三种溶液中溶质质量分数的大小关系为 .
(5)含有少量B的A物质可采用 方法提纯.
【答案】分析:(1)由溶解度曲线直接观察就行;
(2)根据饱和溶液与不饱和溶液的判断方法考虑;
(3)根据溶质质量分数的计算方法考虑;
(4)由t1℃升至 t4℃时三种物质溶质的变化情况考虑;
(5)根据物质提纯的方法考虑.
解答:解:(1)由图示可知只有C的溶解度随温度升高而减小;
(2)在曲线上(或曲线上边的点)都是饱和溶液,在曲线下边的点都是不饱和溶液,t1℃时ag只在曲线C的下边,所以C为不饱和溶液;
(3)由于在t3℃时ABC三种物质的溶解度相等且溶质都为ag,正好达到饱和状态,所以溶质质量分数相等;
(4)若将温度由t1℃升至 t4℃时AB两物质都为不饱和溶液,且溶质都是ag,溶剂都是100g,所以溶质质量分数相同,由于t4℃C的溶解度小于ag,所以C物质会析出晶体,导致溶质减少,所以溶质质量分数减小;
(5)如果溶解度受温度影响较大的物质从溶液中结晶析出的方法是冷却热饱和溶液,如果溶解度受温度影响不大的物质从溶液中结晶析出的方法是蒸发溶剂.由于A物质的溶解度随温度升高变化比较大,所以用冷却热饱和溶液的方法进行提纯.
故答案为:
(1)C;
(2)C;
(3)t3;
(4)A=B>C;
(5)冷却热饱和溶液.
点评:解答本题的关键是要知道溶解度曲线表示的意义,饱和溶液的判断方法,溶质质量分数的判断方法,固体物质从溶液中结晶析出的方法.
(2)根据饱和溶液与不饱和溶液的判断方法考虑;
(3)根据溶质质量分数的计算方法考虑;
(4)由t1℃升至 t4℃时三种物质溶质的变化情况考虑;
(5)根据物质提纯的方法考虑.
解答:解:(1)由图示可知只有C的溶解度随温度升高而减小;
(2)在曲线上(或曲线上边的点)都是饱和溶液,在曲线下边的点都是不饱和溶液,t1℃时ag只在曲线C的下边,所以C为不饱和溶液;
(3)由于在t3℃时ABC三种物质的溶解度相等且溶质都为ag,正好达到饱和状态,所以溶质质量分数相等;
(4)若将温度由t1℃升至 t4℃时AB两物质都为不饱和溶液,且溶质都是ag,溶剂都是100g,所以溶质质量分数相同,由于t4℃C的溶解度小于ag,所以C物质会析出晶体,导致溶质减少,所以溶质质量分数减小;
(5)如果溶解度受温度影响较大的物质从溶液中结晶析出的方法是冷却热饱和溶液,如果溶解度受温度影响不大的物质从溶液中结晶析出的方法是蒸发溶剂.由于A物质的溶解度随温度升高变化比较大,所以用冷却热饱和溶液的方法进行提纯.
故答案为:
(1)C;
(2)C;
(3)t3;
(4)A=B>C;
(5)冷却热饱和溶液.
点评:解答本题的关键是要知道溶解度曲线表示的意义,饱和溶液的判断方法,溶质质量分数的判断方法,固体物质从溶液中结晶析出的方法.

练习册系列答案
相关题目
 17、如图是A、B、C三种固体物质的溶解度曲线示意图,试回答下列问题.
17、如图是A、B、C三种固体物质的溶解度曲线示意图,试回答下列问题. 29、如图是a、b、c三种固体物质的溶解度曲线图.
29、如图是a、b、c三种固体物质的溶解度曲线图. 16、如图是A、B、C三种固体物质的溶解度随温度变化的曲线图.根据图回答:
16、如图是A、B、C三种固体物质的溶解度随温度变化的曲线图.根据图回答: (1)如图是A、B、C三种物质的溶解度曲线.请回答:
(1)如图是A、B、C三种物质的溶解度曲线.请回答:
