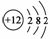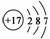题目内容
请根据下图所示的实验过程和提供的数据计算
 |
 +
+
(1)生成氢气 g;
(2)合金中铜的质量分数是 ;
(3)所用稀硫酸的溶质质量分数是多少?(写出计算过程,计算结果保留 到0.1%)
到0.1%)
.解:(1)0 .2g
.2g  1分
1分
(2)35% 1分
(3)生成ZnSO4的质量为100g×16.1%=16.1g
设稀硫酸中硫酸的质量为x
Zn+H2SO4=ZnSO4+H2↑ ............................................... 1分
98 161
x 16.1g
98:x=161:16.1g
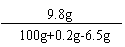 x=9.8g
x=9.8g
.所用稀硫酸的溶质质量分数为 ×100% ≈10.5%
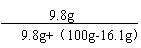
或 ×100% ≈10.5% ................ ......
......

物质X是一种可再生绿色能源,其燃烧的化学方程式为x+3 O2 2CO2+3H2O
2CO2+3H2O
,则X的化学式为( )
| A.C2H4 | B.CH3OH | C.C2H5OH | D.C2H6 |
已知下表信息。
| 名称 | 钠 | 镁 | 铝 | 硅 | 磷 | 硫 | 氯 | 氩 |
| 原子 | ||||||||
| 结构 |
|
|
|
|
|
|
|
|
| 最高 | ||||||||
| 正价 | +1 | +2 | +3 | +4 | +5 | +6 | +7 | |
| 最低 | ||||||||
| 负价 | 无 | 无 | 无 | -4 | -3 | -2 | -1 | 0 |
(1)按照表中排列的递变规律,填写镁元素和氯元素相应的空格。
(2)上表中所有原子的_ _相同,从左到右,_ _、_ _、_ _依次递增。
(3)金属元素的原子最外层电子数一般_ _,非金属元素的原子最外层电子数一般_ _。
(4)元素的最高正化合价等于_ _,稀有气体元素氩的化合价一般为零,表明氩原子结构是一种_ _。
(5)金属元素_无_负价,非金属元素_ _负价。原因是_ _。
(6)非金属元素的最低负价数等于_ _。
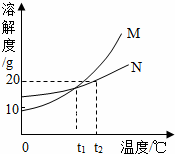

 合金属放入足量的盐酸中充分反应,然后过滤,剩余的固体应该有的金属是
合金属放入足量的盐酸中充分反应,然后过滤,剩余的固体应该有的金属是