题目内容
9.如表是部分物质的溶解性表(室温),利用表中提供的信息回答下列问题:(1)酸、碱、盐之间发生的复分解反应,其实质是它们的溶液中离子之间相互结合生成沉淀或气体或水,否则反应就不能发生.则BaCl2溶液和NaNO3溶液混合后,不能(填“能”或“不能”)发生复分解反应.
(2)写出一个有BaSO4生成的中和反应化学方程式H2SO4+Ba(OH)2=BaSO4↓+2H2O.
| OH- | NO3- | Cl- | SO42- | |
| H+ | - | 溶、挥 | 溶、挥 | 溶 |
| Na+ | 溶 | 溶 | 溶 | 溶 |
| Ca2+ | 溶 | 溶 | 溶 | 微 |
| Ba2+ | 溶 | 溶 | 溶 | 不 |
分析 (1)酸、碱、盐之间发生复分解反应的实质是离子之间的互换反应,两种离子若能结合成沉淀、气体或水,反应便能发生,据此进行分析判断;
(2)可根据经验:硫酸或可溶性硫酸盐的鉴定方法,滴加氯化钡溶液生成不溶于水和酸的硫酸钡沉淀.也可通过以下分析解答:根据复分解反应发生的特点,生成硫酸钡则反应物应为可溶性含钡化合物即可溶性钡盐或氢氧化钡、可溶性的含硫酸根的化合物即硫酸或榀溶性硫酸盐.然后结合题中溶解性表找出符合要求的物质.
解答 解:(1)由于复分解是交换阴阳离子,BaCl2与NaNO3交换成分后对应的是硝酸盐(硝酸钡)和钠盐(氯化钠),而硝酸盐和钠盐均是可溶性盐,不能发生反应,
故填:不能;
(2)中和反应是指酸和碱反应生成盐和水的反应,生成物为硫酸钡,所以酸为硫酸,碱为氢氧化钡,该反应的化学方程式为H2SO4+Ba(OH)2=BaSO4↓+2H2O.
故填:H2SO4+Ba(OH)2=BaSO4↓+2H2O.
点评 本题难度不大,考查同学们灵活运用复分解反应发生的条件来判断物质之间能否发生复分解反应的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19. 将质量相等的铁片插入装有相同质量的稀H2SO4,FeSO4溶液、CuSO4溶液中,随着反应的进行中,三种溶液的质量变化如图所示,则a、b、c三条线表示的溶液为( )
将质量相等的铁片插入装有相同质量的稀H2SO4,FeSO4溶液、CuSO4溶液中,随着反应的进行中,三种溶液的质量变化如图所示,则a、b、c三条线表示的溶液为( )
 将质量相等的铁片插入装有相同质量的稀H2SO4,FeSO4溶液、CuSO4溶液中,随着反应的进行中,三种溶液的质量变化如图所示,则a、b、c三条线表示的溶液为( )
将质量相等的铁片插入装有相同质量的稀H2SO4,FeSO4溶液、CuSO4溶液中,随着反应的进行中,三种溶液的质量变化如图所示,则a、b、c三条线表示的溶液为( )| A. | CuSO4、FeSO4、H2SO4 | B. | FeSO4、CuSO4、H2SO4 | ||
| C. | H2SO4、FeSO4、CuSO4 | D. | H2SO4、CuSO4、FeSO4 |
20.已知硝酸钾的溶解度随温度升高而增大,把一定量50℃的硝酸钾饱和溶液降温至30℃时,肯定不变的是( )
| A. | 溶质的质量 | B. | 溶液的质量 | ||
| C. | 溶液中溶质的质量分数 | D. | 溶剂的质量 |
4.向含CaCl2、HCl二种溶质的溶液中加入10%的Na2CO3溶液实验过程中,加入Na2CO3溶液与产生沉淀或气体的关系如图1所示,加入Na2CO3溶液与溶液PH值变化如图2所示,则下列说法正确的是( )
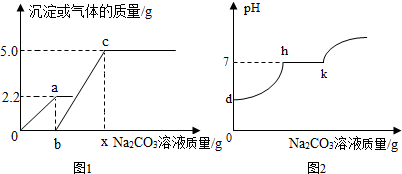

| A. | 图1中b→c段表示生成气体的过程 | |
| B. | 图1中b点的值为106 | |
| C. | 图1中c时溶液中有二种溶质 | |
| D. | 图1中0→a段反应过程中溶液PH值变化过程可用图2中d→h段表示 |
14.善于归纳有利于培养思维能力.其中归纳有错误的一组是( )
| A.日常生活经验 | B.元素与人体健康 |
| ①除去衣服上的油污:用汽油洗涤 ②区别硬水和软水:常用肥皂水检验 ③煤火取暧防中毒:保持室内通风 | ①缺铁:易引起贫血 ②缺钙:易得佝偻病或骨质疏松 ③缺硒:可能引起表皮角质化和癌症 |
| C.生活中的安全常识 | D.化学实验数据记录 |
| ①瓦斯爆炸:由甲烷引起 ②煤气中毒:由一氧化碳引起 ③工业用盐中毒:由亚硝酸钠引起 | ①用10mL量筒量取7.25mL水 ②用pH试纸测得某地水的pH为5.2 ③用托盘天平称得某小苏打样品的质量为16.7g |
| A. | A | B. | B | C. | C | D. | D |
1.聚乳酸,一种可降解塑料,可用作包装材料、纤维和非织造物等.聚乳酸塑料属于( )
| A. | 无机非金属材料 | B. | 金属材料 | C. | 合成材料 | D. | 复合材料 |
16.锰与氧化铁的反应属于( )
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
 污染药品
污染药品 污染药品
污染药品 造成药品变质
造成药品变质 损坏试管.
损坏试管.