题目内容
有铜粉和铁粉的混合20克与90.8克稀盐酸恰好完全反应,得到标准状况下的氢气4升(在标准状况下,氢气的密度为0.09克/升),求混合物中含铁的质量分数.
生成氢气的质量为0.09克/升×4=0.36g.
设参加反应的铁粉的质量为x,
Fe+2HCl═FeCl2+H2↑
56 2
x 0.36g
=
x=10.08g
混合物中含铁的质量分数为
×100%=50.4%.
答:混合物中含铁的质量分数为50.4%.
设参加反应的铁粉的质量为x,
Fe+2HCl═FeCl2+H2↑
56 2
x 0.36g
| 56 |
| 2 |
| x |
| 0.36g |
混合物中含铁的质量分数为
| 10.08g |
| 20g |
答:混合物中含铁的质量分数为50.4%.

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
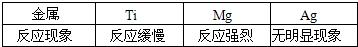
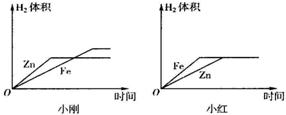
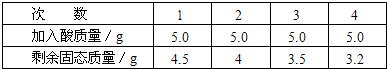
 (2013?下城区二模)某兴趣小组探究金属的反应规律.
(2013?下城区二模)某兴趣小组探究金属的反应规律.