题目内容
将6g碳与一定量的氧气在密闭容器中加高温使其充分燃烧,生成18g气体,则该气体是________;其质量分别是________。
答案:
解析:
提示:
解析:
| 精析 碳在氧气中燃烧,因参加反应的物质的质量不同,就会有CO和CO2两种产物。如果已知参加反应的碳和氧气的质量,从它们的质量比入手,就可以判断出其燃烧的产物。
1.假设碳和氧气反应生成CO,根据化学反应方程式 2C+O2 24 32 可知:参加反应的碳和氧气的质量比为 m(C)∶m(O2)=24∶32=3∶4 在上述反应中,若碳过量其产物仍然是CO,而此时m(C)∶m(O2)>3∶4(多余的碳会跟CO2反应,生成CO)。 结论①:当m(C)∶m(O2)³3∶4时,碳的燃烧产物是CO。 2.假设碳和氧气反应生成CO2,根据化学反应方程式 C+O2 12 32 m(C)∶m(O2)=12∶32=3∶8,碳可充分燃烧生成CO2。 结论②:m(C)∶m(O2)£3∶8时,碳的燃烧产物是CO2。 结论③:3∶8<m(C)∶m(O2)<3∶4时,碳的燃烧产物是CO和CO2的混合物。 根据以上结论①②③解例题: 根据质量守恒定律可知,参加反应的氧气质量是18g-6g=12g,则m(C)∶m(O2)=6∶12=3∶6,根据结论③可知这18g气体是CO和CO2的混合气体。 设18g气体中CO2的质量为x。 则有 x=11g,则CO质量为(18-11)g=7g 答案 CO与CO2的混合气体 CO∶7g,CO2∶11g
|
提示:

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
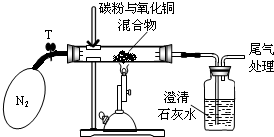 某学习小组对炭粉与氧化铜高温反应产物中气体的成分进行研究.
某学习小组对炭粉与氧化铜高温反应产物中气体的成分进行研究.【猜想】
①气体产物全部是CO2②气体产物是
若猜想①成立,则碳和氧化铜高温反应的化学方程式为:
【设计方案】将一定量氧化铜在隔绝氧气的条件下与过量的炭粉完全反应,测定参加反应的碳元素与氧元素的质量比.
【查阅资料】氮气不与碳、氧化铜产生反应,可用来隔绝氧气.
【实验】
| 操作步骤及实验现象 | 简答 |
| ①称取8g氧化铜与2g碳粉均匀混合,放入重48.4g的玻璃管中,按上图装置连接 | / |
| ②加热前,先通一段时间纯净、干燥的氮气 | 其目的是 |
| ③夹紧T处弹簧夹,加热一段时间,澄清石灰水变浑浊 | 澄清石灰水变浑浊的化学方程式为: |
| ④完全反应后,冷却至室温,称得玻璃管和固体的总质量为56.0g | / |
【结论】根据数据处理结果,得出猜想