题目内容
13. 酸和碱能发生中和反应,生成盐和水.
酸和碱能发生中和反应,生成盐和水.(1)已知甲、乙分别是盐酸和氢氧化钠溶液中的一种,图中表示向甲中加入乙时溶液pH的变化曲线,请你写出图中所获取的4条信息甲溶液为盐酸,乙是氢氧化钠溶液;C点pH值为7,二者恰好中和.
(2)试列举中和反应在生产生活的应用用熟石灰改良酸性土壤.
分析 (1)根据图象中pH值的变化关系,确定甲乙溶液的名称,并根据图象变化及相关知识确定获得的信息;
(2)根据中和反应的实质进行分析,中和反应是酸和碱的反应,所举的例子是酸和碱的反应即可.
解答 解:(1)图象中的pH值的起点小于7,说明甲溶液显酸性,为盐酸,则乙是氢氧化钠溶液;随着加入的乙的量的增加,pH值逐渐增大,与7相交的地方即C点pH值为7,二者恰好中和;
(2)中和反应是指酸与碱生成盐和水的反应.生产生活中应用有很多,例如:用熟石灰改良酸性土壤、炼制石油时残留的硫酸能用氢氧化钠溶液中和或稀氨水处理蚊虫叮咬过的皮肤等;
故答案为:(1)甲溶液为盐酸,乙是氢氧化钠溶液;C点pH值为7,二者恰好中和;
(2)用熟石灰改良酸性土壤.
点评 本题主要考查了学生依据溶液的pH值变化并结合图象分析、解决问题的能力,难度适中,开放性强.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.鉴别下列各组物质,所用试剂或方法不正确的是( )
| A. | 铜粉和氧化铁粉末-稀硫酸 | B. | 稀盐酸和碳酸钠溶液-酚酞试液 | ||
| C. | 氯化钠粉末和硝酸铵粉末-水 | D. | 氮气和二氧化碳-燃着的木条 |
12.下列符合号表示2个氧原子的是( )
| A. | 2O | B. | O2 | C. | O2- | D. | O22- |
1.在100升空气里氧气的体积大约是( )
| A. | 78升 | B. | 78% | C. | 21升 | D. | 21% |
8.暑假,同学们在帮忙老师整理实验室时,发现一瓶石灰水试剂瓶瓶壁和瓶塞周围有一些白色粉末.为了弄清楚白色粉末的成分及形成原因,他们进行了如下探究:
(1)对白色粉末成分的猜想和成因分析:
经过反复思考,同学们认为白色粉末还可能是CaCO3和Ca(OH)2的混合物.
(2)设计实验:
甲同学取白色粉末装入试管中,加入少量的水、振荡,发现有白色固体不溶解.于是他得出粉末中一定有CaCO3的结论.乙同学查阅了溶解性表(如下表),认为甲同学的结论不严密,理由是:Ca(OH)2微溶于水.
为了得出较严密的结论,他们进行了如下实验:
请完成下列实验报告:
(3)交流与反思:
①通过上述实验的探究,同学们向实验室提出保存、使用易变质的溶液时的下列建议,合理的是AB(选填序号).
A.密封保存 B.使用前,临时配制 C.禁止使用这种试剂
②实验室清洗装石灰水试剂瓶内壁上的白色粉末时,可用稀盐酸,请写出其中可能发生的反应的化学方程式(写出一个即可):CaCO3+2HCl=CaCl2+H2O+CO2↑.
(1)对白色粉末成分的猜想和成因分析:
| 白色粉末的成分 | 形成的原因 |
| 可能是CaCO3 | 石灰水与空气中CO2反应; 化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O |
| 可能是Ca(OH)2 | 暑假气温较高,溶质的溶解度降低或溶剂蒸发,石灰水中的溶质结晶析出 |
(2)设计实验:
甲同学取白色粉末装入试管中,加入少量的水、振荡,发现有白色固体不溶解.于是他得出粉末中一定有CaCO3的结论.乙同学查阅了溶解性表(如下表),认为甲同学的结论不严密,理由是:Ca(OH)2微溶于水.
| OH- | Cl- | CO32- | NO3- | |
| Ca2+ | 微 | 溶 | 不 | 溶 |
请完成下列实验报告:
| 实验步骤 | 可能观察到的现象 | 结论 |
| 取上述试管中的上层清液,滴加1~2无色酚酞试液 | 酚酞试液变红色 | 白色粉末中有Ca(OH)2 |
| 往上述试管中的残留的固体中加入稀盐酸 | 有气泡产生 | 白色粉末中有(选填“有”或“无”)CaCO3 |
| 由上述实验可知白色粉末的成分是:Ca(OH)2和CaCO3的混合物. | ||
①通过上述实验的探究,同学们向实验室提出保存、使用易变质的溶液时的下列建议,合理的是AB(选填序号).
A.密封保存 B.使用前,临时配制 C.禁止使用这种试剂
②实验室清洗装石灰水试剂瓶内壁上的白色粉末时,可用稀盐酸,请写出其中可能发生的反应的化学方程式(写出一个即可):CaCO3+2HCl=CaCl2+H2O+CO2↑.
2.下列实验操作中,正确的是( )
| A. | 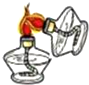 | B. |  | C. |  | D. | 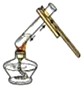 |
3.下列变化中,与其他三种变化有本质不同的是( )
| A. | 钢铁生锈 | B. | 食物腐败 | C. | 汽车轮胎爆炸 | D. | 烧制陶器 |
