题目内容
3.某实验室需要用氧气做实验.现将28.6g氯酸钾与5.4g的二氧化锰混合加热一定时间后,冷却称得剩余固体为25.6g,请计算:(1)制得的氧气质量为8.4g.
(2)剩余固体中存在哪些质?各多少克?
分析 将28.6克氯酸钾和5.4克二氧化锰的混合物加热到一定时间后,冷却称量剩余固体为25.6g,由质量守恒定律,固体混合物减少的质量即为生成氧气的质量;由氧气的质量、反应的化学方程式计算出生成氯化钾的质量,据此进行分析解答.
解答 解:(1)由质量守恒定律,生成氧气的质量为28.6g+5.4g-25.6g=8.4g.
设生成氯化钾的质量为x
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
149 96
x 8.4g
$\frac{149}{96}=\frac{x}{8.4g}$
x=13.04g
二氧化锰作催化剂,反应前后质量不变,剩余固体中氯化钾和二氧化锰的质量为13.04g+5.4g=18.44g;则剩余固体中剩余氯酸钾的质量为25.6g-18.44g=7.16g.
答:(1)8.4g;
(2)剩余固体中存在氯酸钾、氯化钾和二氧化锰,其质量分别是7.16g、13.04g、5.4g.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算出氧气的质量是正确解答本题的前提和关键.

练习册系列答案
相关题目
4.采取正确的措施,能够避免火灾发生或减少灾害损失.下列灭火方法不恰当的是( )
| A. | 油锅起火--用锅盖盖灭 | B. | 酒精灯着火--用湿抹布盖灭 | ||
| C. | 汽车油箱着火--用水浇灭 | D. | 森林起火--砍伐树木形成隔离带 |
5.科学家最新发现,通过简单的化学反应,可以将树木纤维素转变为超级储能装置,该反应的微观示意图如图,下列说法正确的是( )
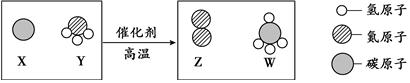

| A. | Y是由四种元素组成的化合物 | |
| B. | 该反应中X、Z两种物质的质量比为3:14 | |
| C. | 该反应中生成的Z和W两物质的分子个数比为1:1 | |
| D. | 参加反应的Y中氮元素的质量一定等于生成Z的质量 |
2.在一定条件下,一个密闭容器内发生某反应,测得反应前后各物质的质量如表所示.下列有关说法不正确的是( )
| 物 质 | a | b | c | d |
| 反应前的质量/g | 30 | 20 | 8 | 14 |
| 反应后的质量/g | x | y | 0 | 10 |
| A. | 参加反应的c与d的质量比为2:1 | B. | x+y=62 | ||
| C. | x的取值范围必须是0≤x≤30 | D. | 当y≤20时,该反应一定是化合反应 |
 小明绘制的两种固体物质的溶解度曲线如图所示:
小明绘制的两种固体物质的溶解度曲线如图所示: 在天平两端各放等质量的两个锥形瓶(瓶口用单孔塞和导管连接起来,气球中装有等质量的大理石),如图所示.左盘锥形瓶中盛有M 克水,右盘锥形瓶中盛有M 克稀盐酸,天平平衡.
在天平两端各放等质量的两个锥形瓶(瓶口用单孔塞和导管连接起来,气球中装有等质量的大理石),如图所示.左盘锥形瓶中盛有M 克水,右盘锥形瓶中盛有M 克稀盐酸,天平平衡.