题目内容
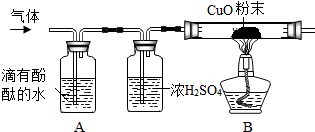
5.请结合下列常用的仪器和装置,回答有关问题:
(1)某兴趣小组同学用加热氯酸钾(KClO3)和二氧化锰的固体混合物来完成实验室制取氧气的基础实验:
①写出用加热氯酸钾(KClO3)和二氧化锰的固体混合物制取氧气的有关反应的化学方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.其发生装置应选用图中的ADFH(填标号)仪器组合,请从所选的装置组合中选择一种玻璃仪器,写出它的名称酒精灯(或试管),简要说出它的用途用作热源(或用作少量试剂的反应容器).
②用BGHI仪器组合装置收集氧气时,验满的方法是当观察到集气瓶内水已排尽,且瓶外有大量气泡冒出时,则证明氧气已收集满;为了使收集到的氧气较为纯净,需等到该组合装置G中导管口冒出的气泡连续并均匀时,才开始收集氧气.
(2)兴趣小组同学想回收上述实验中所得到的固体剩余物,践行节约和环保理念,设计了如图所示实验操作流程.
查阅资料:氯化钾可溶于水,二氧化锰不溶于水.

①在回收提纯的过程中需要控制水的用量,原因有ac(填标号).
a.提高实验效率 b.保证固体1全部溶解 c.节约能源
②步骤Ⅲ中用酸化的硝酸银(AgNO3)溶液检验洗出液中是否含有氯化钾,当观察到有白色沉淀产生,说明洗出液中含有氯化钾.
③步骤Ⅳ中的操作n应选择如图中乙(选填“甲”或“乙”)装置,该操作中玻璃棒不断搅拌的目的是防止加热时局部温度过高而造成液滴飞溅.

④实验结束后,称得回收到的氯化钾的质量比理论值小,可能的原因有蒸发过程中,氯化钾固体飞溅(写一点).
分析 (1)
①根据用氯酸钾制氧气就需要加热,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气解答;
②根据排水法验满的方法及排水法收集氧气的注意事项解答;
(2)加入水溶解氯化钾,且后来需要蒸发水得到氯化钾晶体;根据过滤操作和蒸发操作分析解答;根据硝酸银与氯化钾反应生成氯化银沉淀和硝酸钾氯解答即可.根据实际回收的氯化钾的质量比理论值低,原因可能是:在蒸发的过程中,有少部分氯化钾残留到蒸发皿中解答.
解答 解:
(1)①如果用氯酸钾制氧气就需要加热,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,反应的化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;其发生装置应选用图中的ADFH;酒精灯(或试管); 用作热源(或用作少量试剂的反应容器 );
②用BGHI仪器组合装置收集氧气时,验满的方法是当观察到集气瓶内水已排尽,且瓶外有大量气泡冒出时,则证明氧气已收集满;用G装置收集氧气,当导管口开始有气泡冒出时,不能立即收集,原因是因为装置中有空气;导管口冒出的气泡连续并均匀时,才开始收集氧气;
(2)①在回收提纯的过程中需要控制水的用量,原因有提高实验效率,且后来需要加热蒸发水分,能节约能源;故填:ac;
②硝酸银与氯化钾反应生成氯化银沉淀和硝酸钾,化学方程式:AgNO3+KCl=AgCl↓+KNO3;步骤Ⅲ中用酸化的硝酸银(AgNO3)溶液检验洗出液中是否含有氯化钾,当观察到有白色沉淀产生,说明洗出液中含有氯化钾.
③步骤Ⅳ中的操作n是蒸馏,应选择如图中乙装置,该操作中玻璃棒不断搅拌的目的是防止加热时局部温度过高而造成液滴飞溅;
④称得回收的氯化钾的质量比理论值小,可能的原因有蒸发过程中氯化钾飞溅;
答案:
(1)①2KClO3 $\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;ADFH;酒精灯(或试管); 用作热源(或用作少量试剂的反应容器 );
②当观察到集气瓶内水已排尽,且瓶外有大量气泡冒出时,则证明氧气已收集满;导管口冒出的气泡连续并均匀;
(2)①ac; ②白色沉淀; ③乙;防止加热时局部温度过高而造成液滴飞溅; ④蒸发过程中,氯化钾固体飞溅(或部分氯化钾残留在固体2中或其它合理答案均可).
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的验满等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 阅读快车系列答案
阅读快车系列答案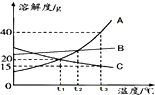
| A. | 温度高于t2℃时,A溶液的溶质质量分数大于B溶液的溶质质量分数 | |
| B. | 要从混有少量B的A溶液中提纯A晶体,操作步骤有蒸发浓缩、降温结晶、过滤等 | |
| C. | t1℃时,将15gA与50g水混合,可以得到65gA溶液 | |
| D. | t3℃时,将饱和的A、B溶液降温至t2℃,析出晶体量A大于B |
| A. |  | B. |  | C. |  | D. |  |
| A. |  用玻璃棒制作的集气瓶 | B. |  用不锈钢制作的坩埚钳 | ||
| C. |  用塑料制作的药匙 | D. |  用铁丝和石棉的石棉网 |
| A. | 二氧化硫通入稀高锰酸钾溶液中,溶液褪色 | |
| B. | 浓硝酸滴入蛋清溶液中,微热,出现黄色沉淀 | |
| C. | 铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 | |
| D. | 二氧化碳通入氯化钙溶液中,产生白色沉淀 |

 某造纸厂排放的废水中含有Na2CO3和NaOH.为了测定废水中Na2CO3的质量分数,取废水100g,逐滴加入稀盐酸至过量,测得生成气体质量与所加稀盐酸质量关系如下图所示:请回答下列问题:
某造纸厂排放的废水中含有Na2CO3和NaOH.为了测定废水中Na2CO3的质量分数,取废水100g,逐滴加入稀盐酸至过量,测得生成气体质量与所加稀盐酸质量关系如下图所示:请回答下列问题: