题目内容
向CuO和铁粉的混合物中加入一定量的稀硫酸,微热,充分反应后冷却、过滤,在滤液中放入一枚洁净的铁钉.发现铁钉表面无任何变化,据此判断,下列结论正确的是( )
A.滤液中一定含有FeSO4,可能含有H2SO4
B.滤液中可能有CuSO4
C.滤渣里一定有Cu,可能有Fe和CuO
D.滤渣里一定有Cu和Fe
【考点】酸的化学性质;金属的化学性质.
【专题】常见的酸 酸的通性.
【分析】根据金属活动顺序可知向滤液中加入薄铁片,而氧化铜可以和硫酸反应生成硫酸铜,铁可以硫酸铜反应铁片无任何变化,说明没有稀硫酸,也没有硫酸铜可以据此结合题给的选项进行分析判断即可;
【解答】解:A、铁可以和硫酸反应生成FeSO4,所以在滤液中一定含有FeSO4,但是加入铁钉后铁片没有明显变化,所以可以判断滤液中没有H2SO4,故A结论不正确;
B、在滤液中放入一枚洁净的铁钉.发现铁钉表面无任何变化,所以可以判断滤液中没有CuSO4,故B结论不正确;
C、加入铁钉后没有明显变化,说明氧化铜和硫酸反应生成的硫酸铜被铁置换出来,故在不溶物中含有Cu,如果硫酸的量不足,那么滤渣里就可能有Fe和CuO,故C结论正确;
D、加入铁钉后没有明显变化,说明氧化铜和硫酸反应生成的硫酸铜被铁置换出来,故在不溶物中含有Cu,题中没有提及铁粉的质量,所以反应后滤出的不溶物中可能含有Fe也可能不含Fe,故D结论不正确.
故选C.
【点评】此题是一道推断知识考查题,解题的关键是对最后加入铁后无变化的分析,也就是说明反应后的溶液中不会有硫酸铜及硫酸的存在,这是解题的关键.

 名校课堂系列答案
名校课堂系列答案20℃时,取甲、乙、丙、丁四种纯净物各40g,分别加入到四个各盛有100g水的烧杯中,充分溶解,其溶解情况如表所示:下列说法正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 未溶解固体的质量/g | 8.4 | 4 | 0 | 18.4 |
A.所得四杯溶液都是饱和溶液
B.四被杯溶液中溶质质量分数关系为:丁>甲>乙>丙
C.升高温度,四杯溶液中溶质的质量分数一定会改变
D.20℃时,分别向四个烧杯中再加入100g水,所得溶液的质量相等,且均为不饱和溶液
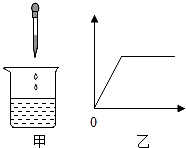
向烧杯中逐滴加入X溶液至过量(图甲),生成沉淀或气体的质量(纵坐标)与加入X溶液的质量(横坐标)关系不符合图乙的是( )
| 烧杯中的物质 | X溶液 | |
| A | 稀硫酸 | 氯化钡溶液 |
| B | 稀硫酸和硫酸铜溶液 | 氢氧化钠溶液 |
| C | 氯化钙溶液 | 碳酸钠溶液 |
| D | 碳酸氢钠溶液 | 稀盐酸 |
A.A B.B C.C D.D


