题目内容
请结合下列实验常用装置,回答有关问题.

(1)写出图中标有数字的仪器名称:①______;②______.
(2)若加热氯酸钾和二氧化锰的混合物制取氧气,应选用的发生装置是______(填“A”或“B”),反应的化学方程式是______.
(3)某同学要用B制得的H2(其中含有水蒸汽),先干燥,再用来检测某铜和铜的氧化物组成的混合物中铜元素的质量分数.称取10.0g样品,进行如图所示的实验.请你将他设计的装置及瓶中所盛物质补画完整.图中试剂a是______;装置G的质量反应前后相差1.8g,(假设所有反应都完全)则样品中铜元素的质量分数为______.

解:(1)根据常用仪器的名称和用途判断可知仪器分别是:长颈漏斗、水槽;
故答案为:长颈漏斗;水槽;
(2)加热氯酸钾和二氧化锰的混合物制取氧气属于“固体加热型”,因此选择A装置,氯酸钾在二氧化锰作催化剂,加热的条件下生成氯化钾和氧气;
故答案为:
A; 2KClO3 2KCl+3O2↑;
2KCl+3O2↑;
(3)干燥氢气可在洗气瓶中放入液体干燥剂,也就是浓硫酸;G装置是用来吸收氢气还原氧化铜生成的水,增加的质量就是反应生成的水的质量,根据反应前后元素的质量不变,水中氧元素的质量就等于氧化铜中氧元素的质量,即样品中氧元素的质量,从而计算出铜元素的质量和铜元素的质量分数.
水中氧元素的质量是:1.8g×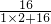 ×100%=1.6g,即样品中氧元素的质量是1.6g,所以铜元素的质量是10g-1.6g=8.4g,
×100%=1.6g,即样品中氧元素的质量是1.6g,所以铜元素的质量是10g-1.6g=8.4g,
所以样品中铜元素的质量分数是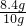 ×100%=84%;
×100%=84%;
故答案为:浓硫酸(或浓H2SO4);图见右(导管长进短出;玻璃管左边要有橡胶胶塞,且导管要略伸出橡胶塞); 84%.

浓硫酸
分析:(1)根据常用仪器的名称和用途判断;
(2)选择发生装置依据反应物的状态和反应条件,并根据氯酸钾分解的反应原理书写化学方程式;
(3)干燥氢气可在洗气瓶中放入液体干燥剂,也就是浓硫酸,并根据元素守恒计算铜元素的质量分数.
点评:本题主要考查了实验室制取气体的装置选取、反应方程式、气体的干燥及计算,考查知识全面,难度稍大.
故答案为:长颈漏斗;水槽;
(2)加热氯酸钾和二氧化锰的混合物制取氧气属于“固体加热型”,因此选择A装置,氯酸钾在二氧化锰作催化剂,加热的条件下生成氯化钾和氧气;
故答案为:
A; 2KClO3
 2KCl+3O2↑;
2KCl+3O2↑;(3)干燥氢气可在洗气瓶中放入液体干燥剂,也就是浓硫酸;G装置是用来吸收氢气还原氧化铜生成的水,增加的质量就是反应生成的水的质量,根据反应前后元素的质量不变,水中氧元素的质量就等于氧化铜中氧元素的质量,即样品中氧元素的质量,从而计算出铜元素的质量和铜元素的质量分数.
水中氧元素的质量是:1.8g×
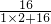 ×100%=1.6g,即样品中氧元素的质量是1.6g,所以铜元素的质量是10g-1.6g=8.4g,
×100%=1.6g,即样品中氧元素的质量是1.6g,所以铜元素的质量是10g-1.6g=8.4g,所以样品中铜元素的质量分数是
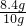 ×100%=84%;
×100%=84%;故答案为:浓硫酸(或浓H2SO4);图见右(导管长进短出;玻璃管左边要有橡胶胶塞,且导管要略伸出橡胶塞); 84%.

浓硫酸
分析:(1)根据常用仪器的名称和用途判断;
(2)选择发生装置依据反应物的状态和反应条件,并根据氯酸钾分解的反应原理书写化学方程式;
(3)干燥氢气可在洗气瓶中放入液体干燥剂,也就是浓硫酸,并根据元素守恒计算铜元素的质量分数.
点评:本题主要考查了实验室制取气体的装置选取、反应方程式、气体的干燥及计算,考查知识全面,难度稍大.

练习册系列答案
相关题目

 ,易溶于水,密度比空气大,常温下在空气中不发生反应.
,易溶于水,密度比空气大,常温下在空气中不发生反应.
 ,易溶于水,密度比空气大,常温下在空气中不发生反应.
,易溶于水,密度比空气大,常温下在空气中不发生反应.