题目内容
12.下列应用和相应的原理(用化学方程式表示)及基本反应类型均正确的是( )| A. | 拉瓦锡测定空气中氧气的含量 4P+5O2$\frac{\underline{\;点燃\;}}{\;}$P2O5 化合反应 | |
| B. | 比较铜和银的金属活动性 Cu+2AgCl═CuCl2+2Ag 置换反应 | |
| C. | 用硫酸除铁锈 Fe2O3+2H2SO4═2FeSO4+3H2O 复分解反应 | |
| D. | 用小苏打制糕点 2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑ 分解反应 |
分析 A、拉瓦锡实验不能测定空气中氧气的含量;
B、铜不能喝氯化银反应;
C、稀硫酸和氧化铁反应生成氯化铁和水;
D、碳酸氢钠受热分解生成碳酸钠、水和二氧化碳.
解答 解:A、虽然磷燃烧生成五氧化二磷,但是拉瓦锡实验不能测定空气中氧气的含量,该选项不正确;
B、虽然铜币银活泼,但是铜和氯化银不能反应,该选项不正确;
C、稀硫酸和氧化铁反应的化学方程式为:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O,该选项不正确;
D、碳酸钠受热分解的化学方程式为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,反应物是一种,生成物是三种,属于分解反应,该选项正确.
故选:D.
点评 书写化学方程式要注意四步:一是反应物和生成物的化学式要正确;二是要遵循质量守恒定律,即配平;三是要有必要的条件;四是看是否需要“↑”或“↓”.

练习册系列答案
相关题目
3.为区别氢氧化钠溶液和澄清石灰水,设计了如下所示四组实验.其中一定能达到目的是( )
| A. |  盐酸 | B. |  氯化铜溶液 | C. |  无色酚酞 | D. |  二氧化碳 |
7.在购买和使用化肥时,要了解化肥的性质,以便合理施用.为了给爸爸做技术指导,小红利用自己掌握的知识对碳酸钾(K2CO3)、硫酸铵[(NH4)2SO4]两种化肥的相关性质做了以下探究.
【实验探究】
【结论与应用】碳酸钾与硫酸铵不能(填“能”或“不能”)混用,说明原因碳酸钾溶液呈碱性,与硫酸铵混合施用,产生NH3,降低肥效.
【实验探究】
| 探 究 过 程 | 实 验 现 象 | 结论及化学方程式 | |
| K2CO3 | (NH4)2SO4 | ||
| (1)配制碳酸钾、硫酸铵溶液.分别取碳酸钾和硫酸铵固体,加足量水搅拌. | 得到澄清溶液,温度无明显变化 | 得到澄清溶液,温度明显降低 | 都易溶于水,硫酸铵溶于水时吸收的热量大于放出的热量. |
| (2)猜想与假设. 碳酸钾、硫酸铵溶液的酸碱性都可能有三种情况. 分别取少量两种溶液于两只试管中,滴加紫色石蕊试液. | 变蓝 | 变红 | 说明碳酸钾溶液显碱性; 说明硫酸铵溶液显 酸 性. |
| (3)与盐酸反应. 分别取少量两种溶液于两只试管中,加入稀盐酸. | 有气泡产生 | 无明显现象 | 碳酸钾能与酸反应. |
| (4)与氢氧化钠溶液反应. 分别取少量两种溶液于两只试管中,加入氢氧化钠溶液,微热. | 无明显现象 | 有气泡产生且有刺激性气味 | 硫酸铵能与碱反应.写出相关的化学方程式:(NH4)2SO4+2NaOH=Na2SO4+2H2O+2NH3↑ |
17.对下列事实的微观解释错误的是( )
| 选项 | 事 实 | 解 释 |
| A | 一氧化碳有毒而二氧化碳无毒 | 两种物质的分子构成不同 |
| B | 品红在热水中扩散速度更快 | 受热情况下,分子运动速率加快 |
| C | 盐酸、稀硫酸都能使紫色石蕊溶液变红 | 两种溶液中都含有氢离子 |
| D | 温度计中的酒精受热膨胀 | 原子间的间隔受热时增大 |
| A. | A | B. | B | C. | C | D. | D |
1.下列运动用品或设施中,主要用到有机合成材料的是( )
| A. | 塑料充气船 | B. | 木制双杠横梁 | C. | 铁合金铅球 | D. | 纯棉护腕 |
 新药帕拉米韦注射液可用于治疗H7N9禽流感,其说明书中部分内容如图
新药帕拉米韦注射液可用于治疗H7N9禽流感,其说明书中部分内容如图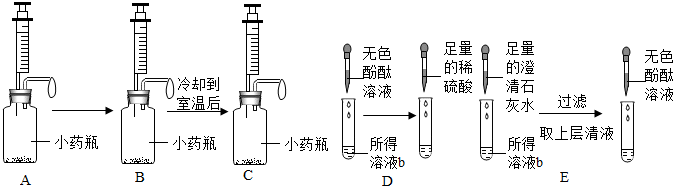
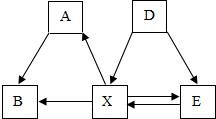 几种常见的物质之间的相互转化关系如图(各字母代表一种物质,各符号表示一个化学反应,部分反应物、生成物及反应条件略去),已知物种物质均有碳、氢、氧中的部分元素组成,A和B所含元素相同,D和E所含元素相同,X为单质,A为有毒气体,B和E可以发生化合反应.
几种常见的物质之间的相互转化关系如图(各字母代表一种物质,各符号表示一个化学反应,部分反应物、生成物及反应条件略去),已知物种物质均有碳、氢、氧中的部分元素组成,A和B所含元素相同,D和E所含元素相同,X为单质,A为有毒气体,B和E可以发生化合反应.