题目内容
20.20℃时,对100g5%的食盐溶液做如下处理,求所得溶液溶质的质量分数(假设每次增加的溶质都完全溶解,列式计算,结果保留一位小数)(1)蒸发20g水后,溶质的质量分数为多少?
(2)增加10gNaCl后,溶质的质量分数为多少?
分析 根据溶液中溶质的质量分数=$\frac{溶质质量}{溶液质量}$×100%分析.
解答 解:20℃时,对100g5%的食盐溶液中溶质质量为5g;
(1)蒸发水20g时溶质质量不变,溶质的质量分数=$\frac{5g}{100g-20g}$×100%=6.25%;
(2)增加10g氯化钠后,则溶质的质量分数=$\frac{5g+10g}{110g}$×100%≈13.6%;
答:(1)蒸发20克水后,所得溶液的溶质质量分数6.25%;
(2)增加10克食盐后,所得溶液的质量分数是13.6%.
点评 此题主要考查溶质质量分数的计算,一定要分清溶质、溶剂、溶液,并准确把握溶质的质量分数这一概念.

练习册系列答案
 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
11.在点燃条件下,A和B反应生成C和D.反应前后分子种类变化的微观示意图如图:以下说法不正确的是( )
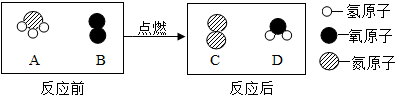

| A. | 这个化学反应共涉及到2种化合物 | |
| B. | 1个A分子中共含有有4个原子 | |
| C. | 在该反应中,生成C和D的质量比为14:27 | |
| D. | 在该反应中,生成C和D的质量比为14:9 |
8.小明在做过滤操作时,在老师给他的仪器中,他认为还缺少一种,其中老师给的仪器主要有:漏斗、烧杯、滤纸、铁架台(带铁圈),那么他认为缺少的仪器是( )
| A. | 小烧杯 | B. | 长颈漏斗 | C. | 药匙 | D. | 玻璃棒 |
9.学习中需要正确理解概念.下列理解正确的是( )
| A. | PH>7的物质一定是碱 | |
| B. | 不能使无色酚酞试液变色的物质一定是酸性的 | |
| C. | 中和反应一定生成盐和水 | |
| D. | 使紫色的石蕊变蓝色溶液一定是酸 |
7. 如图是镁原子的原子结构示意图,下列对镁原子的叙述不正确的是( )
如图是镁原子的原子结构示意图,下列对镁原子的叙述不正确的是( )
 如图是镁原子的原子结构示意图,下列对镁原子的叙述不正确的是( )
如图是镁原子的原子结构示意图,下列对镁原子的叙述不正确的是( )| A. | 镁原子第二电子层有8个电子 | |
| B. | 镁原子最外层电子的能量低于第二层电子的能量 | |
| C. | 镁原子核内有12个质子 | |
| D. | 镁原子在化学反应中容易失去电子 |
