题目内容
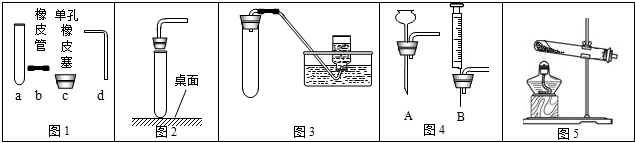
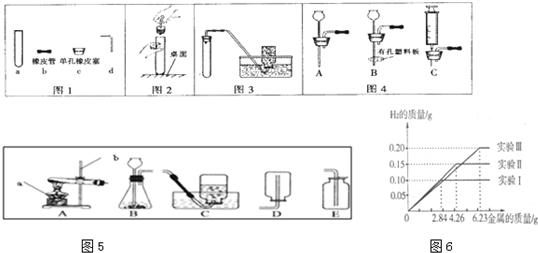
化学是一门以实验为基础的学科,化学所取得的丰硕成果,是与实验的重要作用分不开的.结合下列实验装置图回答问题:

(1)写出图中带标号仪器的名称:①
(2)若实验室对你开放,请从图1中选择固体加热制取气体的装置,制取一种你熟悉的气体.你想制取的气体是
(3)装置B虽然操作简便,但无法控制反应的发生停止.请从图2中选取
(4)用D收集气体时,当导管口气泡
(5)实验室用20g的高锰酸钾制取氧气,反应一段时间后,试管中还剩19.36g固体,请问生成氧气多少克?有多少克高锰酸钾参加了反应?

(1)写出图中带标号仪器的名称:①
酒精灯
酒精灯
,②长颈漏斗
长颈漏斗
.(2)若实验室对你开放,请从图1中选择固体加热制取气体的装置,制取一种你熟悉的气体.你想制取的气体是
氧气
氧气
,反应的化学方程式为2KMnO4
K2MnO4+MnO2+O2↑或2KClO3
2KCl+3O2↑
| ||
| ||
| △ |
2KMnO4
K2MnO4+MnO2+O2↑或2KClO3
2KCl+3O2↑
,检验该气体方法是
| ||
| ||
| △ |
用带火星的木条放在集气瓶口,木条复燃是氧气
用带火星的木条放在集气瓶口,木条复燃是氧气
;选择发生装置的依据是反应条件和反应物的状态
反应条件和反应物的状态
,你所选择的是A
A
(填序号,下同);选择的收集装置是C或D
C或D
,选择此收集装置的理由是氧气密度比空气大且不易溶于水
氧气密度比空气大且不易溶于水
.(3)装置B虽然操作简便,但无法控制反应的发生停止.请从图2中选取
b
b
(填序号)取代B中的单孔塞,以达到控制反应的目的.(4)用D收集气体时,当导管口气泡
连续并均匀放出
连续并均匀放出
时开始收集;当集气瓶口有气泡逸出
集气瓶口有气泡逸出
时表明气体收集满了.(5)实验室用20g的高锰酸钾制取氧气,反应一段时间后,试管中还剩19.36g固体,请问生成氧气多少克?有多少克高锰酸钾参加了反应?
分析:(1)直接写出仪器的名称;
(2)装置A为固固加热型的发生装置,所以可以用来制取氧气;根据氧气能够支持燃烧的性质,可以用带火星的木条来检验该气体;根据反应条件和反应物的状态来选择发生装置;选择气体的收集方法通常根据其密度和水溶性;
(3)根据启普发生器的优点来选择合适的装置;
(4)用排水法收集气体时应该等有连续均匀的气泡冒出时才能收集;
(5)根据质量守恒定律可以求算出生成的氧气的质量,然后根据反应的化学方程式结合氧气的质量可以求算出氯酸钾的质量.
(2)装置A为固固加热型的发生装置,所以可以用来制取氧气;根据氧气能够支持燃烧的性质,可以用带火星的木条来检验该气体;根据反应条件和反应物的状态来选择发生装置;选择气体的收集方法通常根据其密度和水溶性;
(3)根据启普发生器的优点来选择合适的装置;
(4)用排水法收集气体时应该等有连续均匀的气泡冒出时才能收集;
(5)根据质量守恒定律可以求算出生成的氧气的质量,然后根据反应的化学方程式结合氧气的质量可以求算出氯酸钾的质量.
解答:解:(1)直接写出仪器的名称为:①酒精灯;②长颈漏斗;
(2)在制取气体选择发生装置时,通常根据反应物的状态和反应条件来选择发生装置,而装置A为固固加热型的发生装置,而根据我们所学知识可以知道,实验室中用高锰酸钾或氯酸钾制氧气,适合该装置,所以用来制取氧气;根据氧气能够支持燃烧的性质,可以用带火星的木条来检验该气体;氧气的密度比空气大,所以可以选择向上排空气法来收集,而氧气不易溶于水,所以可以选择排水法来收集;
(3)分析图2中装置的特点结合启普发生器的原理可以知道装置b更能适合控制反应的停止和发生;
(4)用排水法收集气体时应该等有连续均匀的气泡冒出时才能收集;
(5)由题意根据质量守恒定律可以求算出生成的氧气的质量是20g-19.36g=0.64g;
设参加反应的高锰酸钾质量为x
2KMnO4
K2MnO4+MnO2+O2↑
316 32
x 0.64g
=
解得:x=6.32g
答:生成氧气的质量是0.64g
故答案为:(1)①酒精灯;②长颈漏斗;
(2)氧气;2KMnO4
K2MnO4+MnO2+O2↑或2KClO3
2KCl+3O2↑; 用带火星的木条放在集气瓶口,木条复燃是氧气;反应条件和反应物的状态;A;C或 D;氧气密度比空气大且不易溶于水;
(3)a;
(4)连续并均匀放出;集气瓶口有气泡逸出.
(5)参加反应的高锰酸钾质量是6.32g.
(2)在制取气体选择发生装置时,通常根据反应物的状态和反应条件来选择发生装置,而装置A为固固加热型的发生装置,而根据我们所学知识可以知道,实验室中用高锰酸钾或氯酸钾制氧气,适合该装置,所以用来制取氧气;根据氧气能够支持燃烧的性质,可以用带火星的木条来检验该气体;氧气的密度比空气大,所以可以选择向上排空气法来收集,而氧气不易溶于水,所以可以选择排水法来收集;
(3)分析图2中装置的特点结合启普发生器的原理可以知道装置b更能适合控制反应的停止和发生;
(4)用排水法收集气体时应该等有连续均匀的气泡冒出时才能收集;
(5)由题意根据质量守恒定律可以求算出生成的氧气的质量是20g-19.36g=0.64g;
设参加反应的高锰酸钾质量为x
2KMnO4
| ||
316 32
x 0.64g
| 316 |
| x |
| 32 |
| 0.64g |
解得:x=6.32g
答:生成氧气的质量是0.64g
故答案为:(1)①酒精灯;②长颈漏斗;
(2)氧气;2KMnO4
| ||
| ||
| △ |
(3)a;
(4)连续并均匀放出;集气瓶口有气泡逸出.
(5)参加反应的高锰酸钾质量是6.32g.
点评:此题考查的是气体的制取原理和装置的选择.只要掌握气体的制取原理,掌握装置选择的依据,问题就能迎刃而解.

练习册系列答案
相关题目
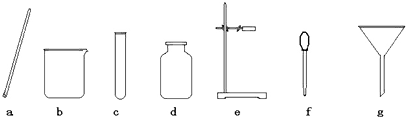
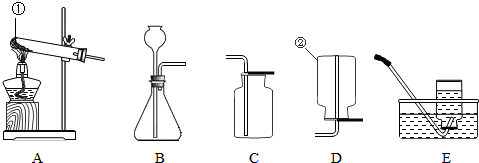
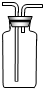
 20、化学是一门以实验为基础的科学,规范的实验操作是实验成功的前提,请回答:
20、化学是一门以实验为基础的科学,规范的实验操作是实验成功的前提,请回答: