题目内容
精盐(NaCl)和纯碱(Na2CO3)是两种常见之物.
(1)用化学方法区别这两种固体,可以选择下列哪一种物质?答:
A.白酒 B.米醋 C.纯净水 D.酱油
(2)王军同学不慎在精盐中混入了少量纯碱,他想重新得到精盐,设计了以下两个实验方案:
方案一:固体混合物
溶液
固体
方案二:固体混合物
溶液
固体
你认为合理的实验方案是 ,反应的化学方程式为
说明另一方案不合理的理由: .
(1)用化学方法区别这两种固体,可以选择下列哪一种物质?答:
A.白酒 B.米醋 C.纯净水 D.酱油
(2)王军同学不慎在精盐中混入了少量纯碱,他想重新得到精盐,设计了以下两个实验方案:
方案一:固体混合物
| 过量稀盐酸 |
| 蒸发 |
方案二:固体混合物
| 过量稀硫酸 |
| 蒸发 |
你认为合理的实验方案是
说明另一方案不合理的理由:
考点:盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的盐 化学肥料
分析:(1)根据纯碱与酸反应会生成二氧化碳气体,而氯化钠不具有此性质进行区分;
(2)根据纯碱能与酸反应,能与稀硫酸反应进行实验方案设计,并从除杂的角度分析不能引入新的杂质进行评价.
(2)根据纯碱能与酸反应,能与稀硫酸反应进行实验方案设计,并从除杂的角度分析不能引入新的杂质进行评价.
解答:解:(1)A、精盐(NaCl)和纯碱(Na2CO3)均溶于白酒,现象相同,故不能用白酒来区分;
B、米醋能够和碳酸钠反应产生二氧化碳,而和氯化钠不反应,因此各取少许精盐和纯碱于试管中,滴入2毫升醋酸,如果有气体产生,证明该物质是纯碱,而另一种物质是精盐,故可以鉴别;
C、精盐(NaCl)和纯碱(Na2CO3)均溶于纯净水,现象相同,故不能用纯净物来区分;
D、精盐(NaCl)和纯碱(Na2CO3)均溶于酱油,现象相同,故不能用酱油来区分.
故选B;
(2)碳酸钠能与盐酸反应生成氯化钠和水,因此固体混合物中加入过量盐酸溶液 过滤,蒸发滤液得到纯净的氯化钠固体;碳酸钠能与稀硫酸反应生成硫酸钠、水和二氧化碳,但会引入新的杂质硫酸钠和过量的硫酸,因此合理的方案是方案一.
故答案为:(1)B;
(2)一; Na2CO3+2HCl═2NaCl+CO2↑+H2O;因为碳酸钠与稀硫酸反应生成了硫酸钠,引入了新杂质.
B、米醋能够和碳酸钠反应产生二氧化碳,而和氯化钠不反应,因此各取少许精盐和纯碱于试管中,滴入2毫升醋酸,如果有气体产生,证明该物质是纯碱,而另一种物质是精盐,故可以鉴别;
C、精盐(NaCl)和纯碱(Na2CO3)均溶于纯净水,现象相同,故不能用纯净物来区分;
D、精盐(NaCl)和纯碱(Na2CO3)均溶于酱油,现象相同,故不能用酱油来区分.
故选B;
(2)碳酸钠能与盐酸反应生成氯化钠和水,因此固体混合物中加入过量盐酸溶液 过滤,蒸发滤液得到纯净的氯化钠固体;碳酸钠能与稀硫酸反应生成硫酸钠、水和二氧化碳,但会引入新的杂质硫酸钠和过量的硫酸,因此合理的方案是方案一.
故答案为:(1)B;
(2)一; Na2CO3+2HCl═2NaCl+CO2↑+H2O;因为碳酸钠与稀硫酸反应生成了硫酸钠,引入了新杂质.
点评:本题是对常见物质的鉴别和除杂的考查,根据物质的不同性质选择合适的试剂出现不同的现象进行鉴别,但在除杂时要注意除杂的原则:不能增加新的杂质,不能减少主体物质.

练习册系列答案
相关题目
下列各组固体物质中只用水不能区分的是( )
| A、碳酸钠 碳酸钙 |
| B、二氧化锰 氧化铜 |
| C、硫酸钡 硝酸钾 |
| D、氯化钠 氯化铁 |
下列物质的用途与性质对应不正确的是
| 物 质 | 用 途 | 性 质 | |
| A | 不锈钢 | 炊具 | 抗腐蚀性 |
| B | 洗涤剂 | 除油污 | 乳化作用 |
| C | 一氧化碳 | 气体燃料 | 可燃性 |
| D | 二氧化碳 | 气体肥料 | 不燃烧、不支持燃烧 |
| A、A | B、B | C、C | D、D |
下列有关实验现象的描述正确的是( )
| A、白磷在空气中燃烧产生大量白雾 |
| B、铁锈与稀盐酸反应后溶液由无色变成了浅绿色 |
| C、硫在空气中燃烧发出微弱的淡蓝色火焰 |
| D、电解水负极得到的气体能使带火星的木条复燃 |
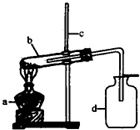 某生设计用高锰酸钾为原料制取氧气的实验装置,回答下列问题:
某生设计用高锰酸钾为原料制取氧气的实验装置,回答下列问题: