题目内容
9.下列仪器不能作为反应容器的是( )| A. | 试管 | B. | 量筒 | C. | 广口瓶 | D. | 烧杯 |
分析 根据已有的仪器的使用方法和注意事项进行分析解答即可,量筒只用于量取液体的体积,不能用作反应的容器,据此解答.
解答 解:A、试管可以用于化学反应的仪器;
B、量筒只用于量取液体的体积,不能用作反应的容器;
C、广口瓶可以用于化学反应的仪器;
D、烧杯可以用于化学反应的仪器;
故选B.
点评 本题考查的是常见的化学仪器的使用方法和注意事项,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
19.食品、生活用品的安全使用问题直接关系到人们的健康.我国禁止含有染色剂“苏丹红一号”(化学式为C16H12N2O)的食品进入市场.下列关于“苏丹红一号”的说法错误的是( )
| A. | “苏丹红一号”是一种有机化合物 | |
| B. | “苏丹红一号”的相对分子质量是248 | |
| C. | “苏丹红一号”中碳元素的质量分数最高 | |
| D. | “苏丹红一号”含有16个碳原子、12个氢原子、2个氮原子和1个氧原子 |
20.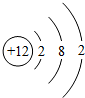 某元素的一种粒子的结构示意图如图所示,下列对该粒子的判断中,错误的是( )
某元素的一种粒子的结构示意图如图所示,下列对该粒子的判断中,错误的是( )
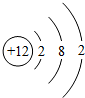 某元素的一种粒子的结构示意图如图所示,下列对该粒子的判断中,错误的是( )
某元素的一种粒子的结构示意图如图所示,下列对该粒子的判断中,错误的是( )| A. | 该粒子是金属元素的原子 | |
| B. | 该元素在化合物中显-2价 | |
| C. | 该元素1个原子的原子核内有12个质子 | |
| D. | 该元素的原子在化学反应中容易失去电子 |
17.在学习酸的性质的实验中,小明发现铁锈与盐酸和铁锈与硫酸反应的速率不同,引发了他的兴趣,于是对“铁锈和酸反应的快慢与什么因素有关”的课题展开探究,如表是他分别用相同质量的铁锈和足量稀盐酸、硫酸反应的实验数据:
(1)写出铁锈与盐酸的反应方程式Fe2O3+6HCl═2FeCl3+3H2O;
(2)实验②和④表明,该反应的快慢与酸的种类有关;
(3)随后他在铁锈与硫酸反应的试管中加入少量盐酸,发现反应明显加快.
【发现问题】为什么反应明显加快呢?
【提出假设】可能是盐酸中某种微粒加快了反应,你猜测是(填盐酸中微粒的符号)H+‘
【设计实验】请设计一个合理的实验来验证你的假设在铁锈与硫酸反应的试管中加入少量氯化钠溶液,观察反应速率的快慢.
(4)铁锈和酸反应的快慢还与什么因素有关?请作出你的假设并设计一个与上述方法不同的实验方案,并写明实验原理.(写出简要的步骤、现象、结论)
| 实验编号 | 盐酸的质量分数/% | 反应温度/℃ | 铁锈消失的时间/s |
| ① | 6 | 20 | 240 |
| ② | 10 | 20 | 115 |
| 实验编号 | 硫酸的质量分数/% | 反应温度/℃ | 铁锈消失的时间/s |
| ③ | 6 | 20 | 310 |
| ④ | 10 | 20 | 155 |
(2)实验②和④表明,该反应的快慢与酸的种类有关;
(3)随后他在铁锈与硫酸反应的试管中加入少量盐酸,发现反应明显加快.
【发现问题】为什么反应明显加快呢?
【提出假设】可能是盐酸中某种微粒加快了反应,你猜测是(填盐酸中微粒的符号)H+‘
【设计实验】请设计一个合理的实验来验证你的假设在铁锈与硫酸反应的试管中加入少量氯化钠溶液,观察反应速率的快慢.
(4)铁锈和酸反应的快慢还与什么因素有关?请作出你的假设并设计一个与上述方法不同的实验方案,并写明实验原理.(写出简要的步骤、现象、结论)
4.空气是混合物,也是一种宝贵资源,空气中各成分有着重要用途.利用空气中各组分性质的差异进行分离,如工业上将空气降温加压使之液化,依据空气中氧气、氮气、稀有气体的沸点不同,控制温度分别汽化,逐一分离.
14.下列变化中,属于化学变化的是( )
| A. | 酒精挥发 | B. | 冰雪融化 | C. | 纸张燃烧 | D. | 矿石粉碎 |
1.小雨阅读课外资料得知:双氧水分解除了用二氧化锰还可用氧化铜等物质作催化剂,于是他对氧化铜产生了探究兴趣.
【提出问题】氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【设计实验】小雨以生成等体积的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略).
(1)上述实验应测量的“待测数据”是收集等量氧气所需时间.
(2)若实验②比实验①的“待测数据”更小 (填“大”或“小”),说明氧化铜能加快氯酸钾的分解速率.
【评价设计】你认为小雨设计实验③和实验②对比的目的是探究氧化铜和二氧化锰哪一个催化效果好.
【提出问题】氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【设计实验】小雨以生成等体积的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略).
| 实验序号 | KClO3质量 | 其他物质质量 | 待测数据 |
| ① | 1.2g | / | |
| ② | 1.2g | CuO 0.5g | |
| ③ | 1.2g | MnO2 0.5g |
(2)若实验②比实验①的“待测数据”更小 (填“大”或“小”),说明氧化铜能加快氯酸钾的分解速率.
【评价设计】你认为小雨设计实验③和实验②对比的目的是探究氧化铜和二氧化锰哪一个催化效果好.
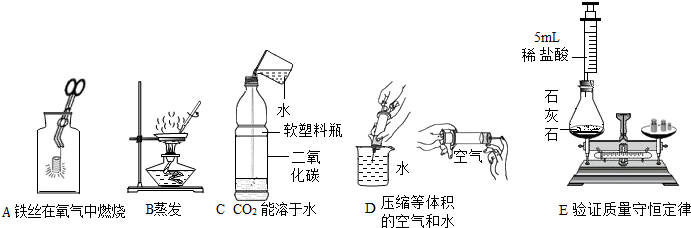
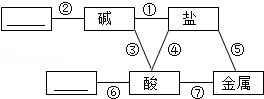 归纳是学习化学的重要方法,总结出如图所示的物质之间的反应关系(图中短线连接的物质表示能相互反应),请帮助完成下列空白:
归纳是学习化学的重要方法,总结出如图所示的物质之间的反应关系(图中短线连接的物质表示能相互反应),请帮助完成下列空白: