题目内容
9.在实验室里加热30g氯酸钾(KClO3)和二氧化锰的混合物制取氧气,完全反应后剩余固体质量为20.4g.请计算:(1)生成氧气的质量为9.6g;
(2)原混合物中二氧化锰的质量.
分析 根据质量守恒定律可知试管内物质质量的减少量就是生成的氧气的质量,根据方程式由氧气的质量,列比例式计算出参加反应的氯酸钾的质量从而可知二氧化锰的质量.
解答 解:(1)由于是完全反应,根据质量守恒,减少的质量就是生成的氧气的质量,即制得氧气:30g-20.4g=9.6g;
(2)设氯酸钾质量为x:
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 96
x 9.6g
$\frac{245}{x}=\frac{96}{9.6g}$
x=24.5g
故混合物中二氧化锰的质量是:30g-24.5g=5.5g
故答案为:(1)9.6;(2)原混合物中二氧化锰的质量为5.5g.
点评 解决本题的关键是要分析出试管内质量的减少量就是生成的氧气质量,再根据氧气质量进行进一步计算.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
18.下列示意图能表示化合物的是( )
| A. |  | B. |  | C. |  | D. |  |
19.检验某气体是否为二氧化碳,常用的方法是( )
| A. | 测量气体的密度 | B. | 将燃烧的木条伸入集气瓶内 | ||
| C. | 将气体通入澄清石灰水 | D. | 将红色的石蕊倒入集气瓶中 |
4.工业上用甲和乙反应制备燃料丙.根据下列微观示意图得出的结论中,正确的是( )


| A. | 甲的化学式为CH2 | |
| B. | 反应中甲、乙、丙的分子个数比为2:1:1 | |
| C. | 甲、乙、丙都可能是氧化物 | |
| D. | 丙中C、H、O元素的质量比12:3:8 |
18.列反应,属于分解反应的是( )
| A. | 铁+氧气$\stackrel{点燃}{→}$四氧化三铁 | |
| B. | 碳酸钙$\stackrel{点燃}{→}$氧化钙+二氧化碳 | |
| C. | 乙醇+氧气$\stackrel{点燃}{→}$二氧化碳+水 | |
| D. | 氯化铁+氢氧化钠=氢氧化铁+氯化钠 |
19.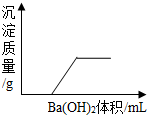 有一溶液是由盐酸、硫酸、稀硝酸、硫酸铁、氯化铁、硝酸铁几种中的两种混合而成,向该溶液中加Ba(OH)2溶液的体积与生成沉淀的质量关系如图所示,则该溶液不可能是以下组合中的( )
有一溶液是由盐酸、硫酸、稀硝酸、硫酸铁、氯化铁、硝酸铁几种中的两种混合而成,向该溶液中加Ba(OH)2溶液的体积与生成沉淀的质量关系如图所示,则该溶液不可能是以下组合中的( )
 有一溶液是由盐酸、硫酸、稀硝酸、硫酸铁、氯化铁、硝酸铁几种中的两种混合而成,向该溶液中加Ba(OH)2溶液的体积与生成沉淀的质量关系如图所示,则该溶液不可能是以下组合中的( )
有一溶液是由盐酸、硫酸、稀硝酸、硫酸铁、氯化铁、硝酸铁几种中的两种混合而成,向该溶液中加Ba(OH)2溶液的体积与生成沉淀的质量关系如图所示,则该溶液不可能是以下组合中的( )| A. | 硝酸、硝酸铁 | B. | 硝酸、硫酸铁 | C. | 盐酸、氯化铁 | D. | 盐酸、硝酸铁 |

