题目内容
计算:(1)化肥硝酸铵(NH4NO3)中氮元素的质量分数.
(2)多少克硝酸铵中含1.4Kg的氮?
(2)多少克硝酸铵中含1.4Kg的氮?
(1)硝酸铵(NH4NO3)中氮元素的质量分数为:
×100%=35%;
(2)含1.4Kg的氮的硝酸铵的质量为:1.4kg÷35%=4kg=4000g.
答:(1)硝酸铵(NH4NO3)中氮元素的质量分数为35%;
(2)4000克硝酸铵中含1.4Kg的氮.
| 14×2 |
| 80 |
(2)含1.4Kg的氮的硝酸铵的质量为:1.4kg÷35%=4kg=4000g.
答:(1)硝酸铵(NH4NO3)中氮元素的质量分数为35%;
(2)4000克硝酸铵中含1.4Kg的氮.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 某化工集团生产的化肥硫酸铵[(NH4)2SO4],含有硫酸钾.其产品包装上标明:硫酸铵[(NH4)2SO4]≥70%.为测定该化肥产品中硫酸铵的质量分数,进行如下实验:取一定量的该化肥配成200g溶液,平均分成两份,(假设所有的反应都是完全反应)
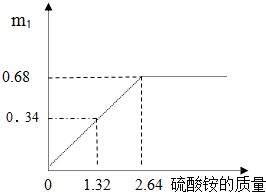
某化工集团生产的化肥硫酸铵[(NH4)2SO4],含有硫酸钾.其产品包装上标明:硫酸铵[(NH4)2SO4]≥70%.为测定该化肥产品中硫酸铵的质量分数,进行如下实验:取一定量的该化肥配成200g溶液,平均分成两份,(假设所有的反应都是完全反应)【实验1】:第1份溶液中加足量KOH溶液,加热,收集到的气体质量m1和(NH4)2SO4的质量关系如右坐标图所示:
【实验 2】:第2份溶液中慢慢滴加硝酸钡溶液后,生成的沉淀和加入的硝酸钡溶液的关系如下表
| 加入硝酸钡溶液质量/g | 10 | 20 | 45 | 55 |
| 产生白色沉淀质量/g | 2、33 | 4、66 | 6、99 | 6、99 |
【实验1】中发生反应的化学方程式为
[实验1]中第1份化肥溶液中硫酸铵的质量为
(1)依据[实验1]和[实验2]有关数据,计算第2份化肥溶液中硫酸钾的质量
(2)该化肥中硫酸铵的质量分数为
 某化工集团生产的化肥硫酸铵[(NH4)2SO4],含有硫酸钾.其产品包装上标明:硫酸铵[(NH4)2SO4]≥70%.为测定该化肥产品中硫酸铵的质量分数,进行如下实验:取一定量的该化肥配成200g溶液,平均分成两份,(假设所有的反应都是完全反应)
某化工集团生产的化肥硫酸铵[(NH4)2SO4],含有硫酸钾.其产品包装上标明:硫酸铵[(NH4)2SO4]≥70%.为测定该化肥产品中硫酸铵的质量分数,进行如下实验:取一定量的该化肥配成200g溶液,平均分成两份,(假设所有的反应都是完全反应)
【实验1】:第1份溶液中加足量KOH溶液,加热,收集到的气体质量m1和(NH4)2SO4的质量关系如右坐标图所示:
【实验 2】:第2份溶液中慢慢滴加硝酸钡溶液后,生成的沉淀和加入的硝酸钡溶液的关系如下表
| 加入硝酸钡溶液质量/g | 10 | 20 | 45 | 55 |
| 产生白色沉淀质量/g | 2、33 | 4、66 | 6、99 | 6、99 |
【实验1】中发生反应的化学方程式为______.
[实验1]中第1份化肥溶液中硫酸铵的质量为______g.
(1)依据[实验1]和[实验2]有关数据,计算第2份化肥溶液中硫酸钾的质量______?
(2)该化肥中硫酸铵的质量分数为______,属______(填“合格或不合格”)产品.
某化工集团生产的化肥硫酸铵[(NH4)2SO4],含有硫酸钾.其产品包装上标明:硫酸铵[(NH4)2SO4]≥70%.为测定该化肥产品中硫酸铵的质量分数,进行如下实验:取一定量的该化肥配成200g溶液,平均分成两份,(假设所有的反应都是完全反应)
【实验1】:第1份溶液中加足量KOH溶液,加热,收集到的气体质量m1和(NH4)2SO4的质量关系如右坐标图所示:
【实验 2】:第2份溶液中慢慢滴加硝酸钡溶液后,生成的沉淀和加入的硝酸钡溶液的关系如下表
回答下列问题:
【实验1】中发生反应的化学方程式为______.
[实验1]中第1份化肥溶液中硫酸铵的质量为______g.
(1)依据[实验1]和[实验2]有关数据,计算第2份化肥溶液中硫酸钾的质量______?
(2)该化肥中硫酸铵的质量分数为______,属______(填“合格或不合格”)产品.

【实验1】:第1份溶液中加足量KOH溶液,加热,收集到的气体质量m1和(NH4)2SO4的质量关系如右坐标图所示:
【实验 2】:第2份溶液中慢慢滴加硝酸钡溶液后,生成的沉淀和加入的硝酸钡溶液的关系如下表
| 加入硝酸钡溶液质量/g | 10 | 20 | 45 | 55 |
| 产生白色沉淀质量/g | 2、33 | 4、66 | 6、99 | 6、99 |
【实验1】中发生反应的化学方程式为______.
[实验1]中第1份化肥溶液中硫酸铵的质量为______g.
(1)依据[实验1]和[实验2]有关数据,计算第2份化肥溶液中硫酸钾的质量______?
(2)该化肥中硫酸铵的质量分数为______,属______(填“合格或不合格”)产品.



