题目内容
用氢气还原一定质量的氧化铜,经一段时间后测得剩余固体混合物中铜占20%,将此固体混合物再用氢气还原,又过了一段时间后测得这次剩余的固体混合物铜占80%,则第二次被还原的氧化铜与第一次被还原的氧化铜的质量比为 .
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据氢气与氧化铜反应的化学方程式,假设一共有氧化铜的质量为a,第一次被还原氧化铜的质量为x,第二次被还原氧化铜的质量为 y,根据铜的质量分数表示出反应的氧化铜的质量.
解答:解:如果第一次说的是铜占20%则
设一共有氧化铜的质量为a,第一次被还原氧化铜的质量为x,第二次被还原氧化铜的质量为 y,
H2+CuO═Cu+H2O
80 64
X
y
(a-x+
)X20%=
①
(a-x-y+
+
)X80%=
+
②
①②解方程的 x=
a,y=
a,
则第二次被还原的氧化铜与第一次被还原的氧化铜质量之比为
=
设一共有氧化铜的质量为a,第一次被还原氧化铜的质量为x,第二次被还原氧化铜的质量为 y,
H2+CuO═Cu+H2O
80 64
X
| 64x |
| 80 |
y
| 64y |
| 80 |
(a-x+
| 64x |
| 80 |
| 64x |
| 80 |
(a-x-y+
| 64x |
| 80 |
| 64y |
| 80 |
| 64x |
| 80 |
| 64y |
| 80 |
①②解方程的 x=
| 5 |
| 21 |
| 25 |
| 42 |
则第二次被还原的氧化铜与第一次被还原的氧化铜质量之比为
| ||
|
| 5 |
| 2 |
点评:本题难度较大,依据化学方程式,解题的关键是根据铜的质量分数表示出反应的氧化铜的质量.

练习册系列答案
 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案
相关题目
一辆客车夜晚行驶在公路上,发现油箱泄漏,车厢里充满了汽油味,这时应该采用的应急措施是( )
| A、洒水降温溶解汽油蒸汽 |
| B、打开所有的车窗,严禁一切烟火,疏散乘客 |
| C、让车内的乘客集中到车厢后部 |
| D、开灯查找漏油部位 |
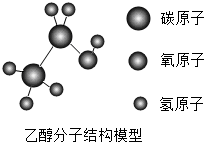 农作物的种子经过发酵、蒸馏制得的乙醇被称为“绿色汽油”.乙醇的分子结构模型如图所示,则下列叙述正确的是( )
农作物的种子经过发酵、蒸馏制得的乙醇被称为“绿色汽油”.乙醇的分子结构模型如图所示,则下列叙述正确的是( )| A、乙醇是由3种元素构成的 |
| B、一个乙醇分子中含有28个质子 |
| C、乙醇中碳、氧元素的质量比为3﹕2 |
| D、乙醇中氧元素的质量分数最大 |