题目内容
某同学取25克碳酸钙加入到100克的稀盐酸中,直到不再产生气体为止,称量反应后剩余物的总质量为116.2克.试计算:
(1)生成二氧化碳的质量为 克.
(2)有多少克的碳酸钙参加了反应?
(3)生成了多少克的氯化钙?
(1)生成二氧化碳的质量为
(2)有多少克的碳酸钙参加了反应?
(3)生成了多少克的氯化钙?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:分析所发生的反应,可发现反应后总质量减轻是由于生成了气体二氧化碳,因此,可知恰好完全反应时放出二氧化碳的质量为8.8g;然后利用二氧化碳的质量,根据反应的化学方程式,分别计算恰好完全反应时碳酸钙的质量和生成氯化钙的质量.
解答:解:
(1)生成二氧化碳的质量=25 g+100 g-116.2 g=8.8 g
设:样品中CaCO3的质量为x,生成氯化钙的质量为y.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 111 44
x y 8.8 g
=
=
x=20g
y=22.2g
答案:
(1)8.8
(2)有20克的碳酸钙参加了反应
(3)生成了22.2克的氯化钙
(1)生成二氧化碳的质量=25 g+100 g-116.2 g=8.8 g
设:样品中CaCO3的质量为x,生成氯化钙的质量为y.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 111 44
x y 8.8 g
| 100 |
| x |
| 111 |
| y |
| 44 |
| 8.8g |
x=20g
y=22.2g
答案:
(1)8.8
(2)有20克的碳酸钙参加了反应
(3)生成了22.2克的氯化钙
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
 用如图所示的简易净水器处理浑浊的河水,下列分析正确的是( )
用如图所示的简易净水器处理浑浊的河水,下列分析正确的是( )| A、净化后的水属于纯净物 |
| B、该净水器能将硬水变为软水 |
| C、该净水器能杀菌消毒 |
| D、用活性炭可以除去水中的色素和异味 |
某学生用量筒量取液体的体积,量筒放平稳且面对刻度线,初次仰视凹液面的最低点读数为19mL,倾出部分液体后,俯视液体凹液面的最低处读数为10mL,则实际该学生倾出液体的体积是( )mL.
| A、9 | B、大于9 |
| C、小于9 | D、无法判断 |
有X、Y、Z三种金属,如果把X、Y和Z分别放入稀硫酸中,X产生气泡的速度明显比Y快,Z无明显变化.根据以上实验事实判断,X、Y、Z三种金属的活动性由强至弱的顺序正确的是( )
| A、X Z Y |
| B、Z Y X |
| C、Y Z X |
| D、X Y Z |
下列微粒符号中,“2”对含义理解正确的是( )
| A、2Cu中的“2”表示2个铜元素 | ||
| B、H2S中的“2”表示一个硫化氢分子中含有2个硫原子 | ||
| C、Fe2+中的“2”表示每个亚铁离子带有2个单位的正电荷 | ||
D、Al2(S
|
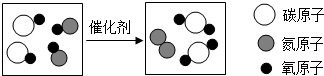 如图是治理汽车尾气反应的微观过程,图中单质是
如图是治理汽车尾气反应的微观过程,图中单质是