题目内容
(6分)为了测定黄铜(铜、锌合金)的组成,某研究性学习小组称取该样品20g,向其中逐滴加入质量分数为19.6%的稀硫酸至刚好不再产生气体为止。反应过程中生成的气体与所用稀硫酸的质量关系如图所示。试计算:
(1)黄铜样品中铜的质量分数;
(2)反应中消耗的稀硫酸的质量;
(3)反应后所得溶液的质量。
(1)解:设合金中锌的质量为x,消耗硫酸的质量为y
Zn + H2SO4 ="=" ZnSO4 + H2↑ 1分
65 98 2
x y 0.2g
65: 2=x:0.2g 解得:x=6.5g 1分
样品中铜的质量分数:[(20g-6.5g)/20g ]×100%=67.5% 1分
(2)65: 2=y:0.2g 解得:y=9.8g 1分
反应中消耗硫酸的质量:9.8g÷19.6%=50g 1分
(3)反应后所得溶液的质量:20g+50g–(20g-6.5g)–0.2g=56.3g 1分
答:略
解析

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案
相关题目
某化学兴趣小组为了测定黄铜(铜、锌合金)中锌的质量分数,取出6g合金样品,将50g稀硫酸分5次加入样品中,充分反应后过滤、洗涤、干燥、称重,得到的实验数据如下:
(1)m值为 ;
(2)求合金中锌的质量分数?
(3)求稀硫酸中溶质的质量分数?
| 稀硫酸用量 | 剩余固体质量 |
| 第一次加入10g | 4.7g |
| 第二次加入10g | mg |
| 第三次加入10g | 2.1g |
| 第四次加入10g | 1.2g |
| 第五次加入10g | 1.2g |
(2)求合金中锌的质量分数?
(3)求稀硫酸中溶质的质量分数?
 为了测定黄铜(铜、锌合金)的组成,某研究性学习小组称取该样品10g,向其中逐滴加入9.8%的稀硫酸至刚好不再产生气体为止.反应过程中生成的气体与所用硫酸溶液的质量关系如图所示.试计算:
为了测定黄铜(铜、锌合金)的组成,某研究性学习小组称取该样品10g,向其中逐滴加入9.8%的稀硫酸至刚好不再产生气体为止.反应过程中生成的气体与所用硫酸溶液的质量关系如图所示.试计算: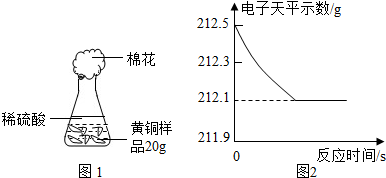
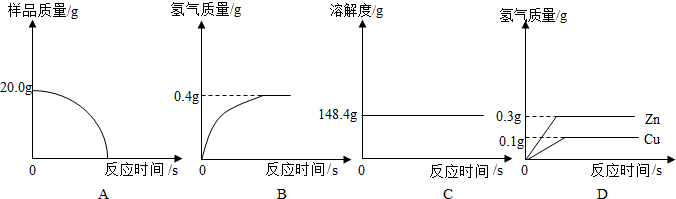
 为了测定黄铜(铜、锌合金)的组成,某研究性学习小组称取该样品10g,向其中逐滴加稀硫酸至刚好不再产生气体为止.反应过程中生成的气体与所用硫酸的质量关系如图所示.根据图示回答问题:
为了测定黄铜(铜、锌合金)的组成,某研究性学习小组称取该样品10g,向其中逐滴加稀硫酸至刚好不再产生气体为止.反应过程中生成的气体与所用硫酸的质量关系如图所示.根据图示回答问题: